Nove publikacije
Zakaj imajo bolniki s pljučnim rakom, ki ne kadijo, slabše rezultate?
Zadnji pregled: 02.07.2025

Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.
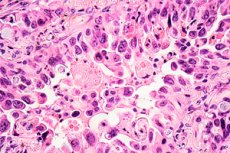
Raziskovalci z University College London (UCL), Francis Crick Institute in AstraZeneca so odkrili razlog, zakaj ciljno usmerjeno zdravljenje nedrobnoceličnega pljučnega raka pri nekaterih bolnikih, zlasti pri tistih, ki niso nikoli kadili, ne deluje.
Študija, objavljena v reviji Nature Communications, kaže, da imajo celice pljučnega raka z dvema specifičnima genetskima mutacijama večjo verjetnost, da podvojijo svojo genomsko obremenitev, kar jim pomaga preživeti zdravljenje in razviti odpornost nanj.
V Združenem kraljestvu je pljučni rak tretja najpogostejša vrsta raka in glavni vzrok smrti zaradi raka. Približno 85 % bolnikov z rakom pljuč ima nedrobnocelični pljučni rak (NSCLC) in je najpogostejša vrsta pri bolnikih, ki niso nikoli kadili. Če ga obravnavamo ločeno, je pljučni rak pri "nikoli kadilcih" peti najpogostejši vzrok smrti zaradi raka po vsem svetu.
Najpogostejša genetska mutacija, ki jo najdemo pri nedrobnoceličnem pljučnem raku (NSCLC), vključuje gen receptorja za epidermalni rastni faktor (EGFR), ki omogoča hitrejšo rast rakavih celic. Najdemo jo pri približno 10–15 % primerov NSCLC v Združenem kraljestvu, zlasti pri bolnikih, ki niso nikoli kadili.
Preživetje je odvisno od stadija raka in le približno tretjina bolnikov z nedrobnoceličnim pljučnim rakom v stadiju IV in mutacijo EGFR preživi tri leta.
Zdravljenja pljučnega raka, ki ciljajo na to mutacijo, znana kot zaviralci EGFR, obstajajo že več kot 15 let. Medtem ko se pri nekaterih bolnikih tumorji raka zmanjšajo z zaviralci EGFR, se drugi bolniki, zlasti tisti z dodatno mutacijo v genu p53 (ki igra vlogo pri zaviranju tumorjev), na zdravljenje ne odzivajo in imajo veliko slabše stopnje preživetja. Vendar znanstveniki in zdravniki niso mogli pojasniti, zakaj je temu tako.
Da bi našli odgovor, so raziskovalci ponovno analizirali podatke iz preskušanj najnovejšega zaviralca EGFR podjetja AstraZeneca, osimertiniba. Pregledali so izhodiščne preiskave in prve kontrolne preiskave, opravljene po več mesecih zdravljenja pri bolnikih z mutacijo EGFR ali mutacijo EGFR in p53.
Ekipa je primerjala vsak tumor na posnetkih, veliko več kot jih je bilo izmerjenih v prvotni študiji. Ugotovili so, da so se pri bolnikih samo z mutacijami EGFR vsi tumorji kot odziv na zdravljenje skrčili. Pri bolnikih z obema mutacijama pa so se nekateri tumorji skrčili, drugi pa so rasli, kar dokazuje hitro odpornost na zdravilo. Ta vrsta odziva, pri kateri se nekatera, ne pa vsa področja raka skrčijo kot odziv na zdravljenje z zdravili pri enem samem bolniku, je znana kot "mešani odziv" in predstavlja izziv za onkologe, ki skrbijo za bolnike z rakom.
Da bi raziskali, zakaj so nekateri tumorji pri teh bolnikih bolj dovzetni za odpornost na zdravila, je ekipa nato preučila mišji model z mutacijami EGFR in p53. Ugotovili so, da je znotraj odpornih tumorjev pri teh miših veliko več rakavih celic podvojilo svojo genomsko obremenitev, kar jim je dalo dodatne kopije vseh kromosomov.
Raziskovalci so nato v laboratoriju zdravili celice pljučnega raka, nekatere z le eno mutacijo EGFR in druge z obema mutacijama, z zaviralcem EGFR. Ugotovili so, da se je po petih tednih izpostavljenosti zdravilu bistveno večji odstotek celic z dvojno mutacijo in dvojnim genomskim bremenom pomnožil v nove celice, ki so bile odporne na zdravilo.
Profesor Charles Swanton z University College London in Francis Crick Institute je dejal: »Pokazali smo, zakaj je mutacija p53 povezana s slabšim preživetjem pri bolnikih z rakom pljuč nekadilcev, ki je kombinacija mutacij EGFR in p53, ki omogoča podvajanje genoma. To poveča tveganje za razvoj celic, odpornih na zdravila, zaradi nestabilnosti kromosomov.«
Bolniki z nedrobnoceličnim pljučnim rakom so že testirani na mutacije EGFR in p53, vendar trenutno ni standardnega testa za odkrivanje prisotnosti podvajanja celotnega genoma. Raziskovalci že iščejo načine za razvoj diagnostičnega testa za klinično uporabo.
Dr. Crispin Highley z University College London in onkološki svetovalec v University Hospitals London je dejal: »Ko bomo lahko identificirali bolnike z mutacijami EGFR in p53, katerih tumorji kažejo podvojitve celotnega genoma, bomo te bolnike lahko zdravili bolj selektivno. To bi lahko pomenilo intenzivnejši nadzor, zgodnejšo radioterapijo ali ablacijo za ciljanje odpornih tumorjev ali zgodnejšo uporabo kombinacij zaviralcev EGFR, kot je osimertinib, z drugimi zdravili, vključno s kemoterapijo.«
