Nove publikacije
Znanstveniki so ustvarili "kameleonsko" spojino za zdravljenje možganskega raka, odpornega na zdravila
Zadnji pregled: 02.07.2025

Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.
Nova študija znanstvenikov z univerze Yale opisuje, kako nova kemična spojina napada možganske tumorje, odporne na zdravila, ne da bi pri tem poškodovala zdravo okoliško tkivo.
Študija, objavljena v reviji Journal of the American Chemical Society, je pomemben korak v razvoju tako imenovanih "kameleonskih spojin", ki bi jih lahko uporabili za boj proti vrsti nevarnih vrst raka.
Gliomi se razvijejo pri približno 6,6 na 100.000 ljudi vsako leto in pri 2,94 na 100.000 ljudi do 14. leta starosti. Če izvzamemo metastaze drugih vrst raka, ki dosežejo osrednji živčni sistem, gliomi predstavljajo 26 % vseh možganskih tumorjev (primarni možganski tumorji) in 81 % vseh malignih možganskih tumorjev.
Bolnike z glioblastomom že desetletja zdravijo z zdravilom temozolomid. Vendar pa večina bolnikov v enem letu razvije odpornost na temozolomid. Petletna stopnja preživetja bolnikov z glioblastomom je manjša od 5 %.
Leta 2022 sta kemik z univerze Yale Seth Herzon in radioonkolog dr. Ranjit Bindra razvila novo strategijo za učinkovitejše zdravljenje glioblastomov. Ustvarila sta razred molekul proti raku, imenovanih kameleonske spojine, ki izkoriščajo napako v proteinu za popravilo DNK, znanem kot O6-metilgvanin DNA metiltransferaza (MGMT).
Številne rakave celice, vključno z glioblastomi, nimajo proteina MGMT. Nove kameleonske spojine so zasnovane tako, da poškodujejo DNK v tumorskih celicah, ki nimajo MGMT.
Kameleonske spojine sprožijo poškodbe DNK z odlaganjem primarnih lezij na DNK, ki se sčasoma razvijejo v zelo strupene sekundarne lezije, znane kot medverižne zamrežitve. MGMT ščiti DNK zdravih tkiv s popravljanjem primarnih lezij, preden se lahko razvijejo v smrtonosne medverižne zamrežitve.
V svoji novi študiji sta se soavtorja Herzon in Bindra osredotočila na svojega glavnega kameleona, KL-50.
»Uporabili smo kombinacijo študij sintetične kemije in molekularne biologije, da bi razjasnili molekularno osnovo naših prejšnjih opazovanj, pa tudi kemijsko kinetiko, ki zagotavlja edinstveno selektivnost teh spojin,« je dejal Herzon, profesor kemije na univerzi Yale, imenovan Milton Harris. »Pokazali smo, da je KL-50 edinstven, saj tvori navzkrižne povezave DNK le v tumorjih z okvarjenim popravilom DNK. Pri tem pa varuje zdravo tkivo.«
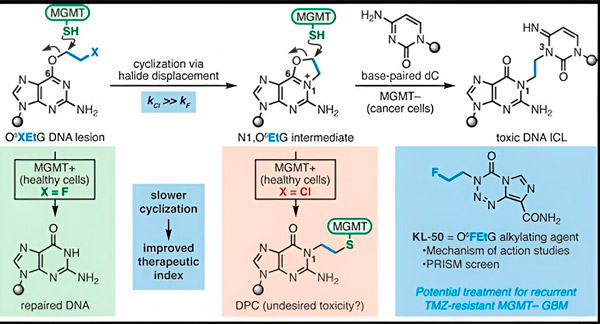
Vir: Časopis Ameriškega kemijskega društva (2024). DOI: 10.1021/jacs.3c06483
To je pomembna razlika, poudarjajo raziskovalci. Številne druge protirakave spojine so bile zasnovane tako, da sprožijo medverižne navzkrižne povezave, vendar niso selektivne za tumorske celice, kar omejuje njihovo uporabnost.
Raziskovalci so ugotovili, da je skrivnost uspeha KL-50 v njegovem času delovanja. KL-50 tvori medverižne zamrežene povezave počasneje kot drugi zamreževalci. Ta zamuda daje zdravim celicam dovolj časa, da uporabijo MGMT in preprečijo nastanek zamreženj.
»Ta edinstven profil kaže na njegov potencial za zdravljenje glioblastoma, odpornega na zdravila, področja z veliko neizpolnjeno potrebo v kliniki,« je dejal Bindra, profesor terapevtske radiologije na Medicinski fakulteti Yale, ki ga vodita Harvey in Kate Cushing. Bindra je tudi znanstveni direktor Centra za možganske tumorje družine Chenevert v bolnišnici Smilo.
Herzon in Bindra sta povedala, da njuna študija poudarja pomen upoštevanja stopenj kemične modifikacije DNK in biokemičnega popravljanja DNK. Verjameta, da lahko to strategijo uporabita za razvoj zdravljenja drugih vrst raka, ki vsebujejo specifične tumorsko povezane napake pri popravljanju DNK.
