Nove publikacije
Preiskava mehanizma izpuščajev zaradi drog na koži
Last reviewed: 02.07.2025

Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.
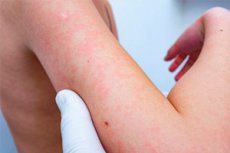
Čeprav zdravila pogosto pomagajo bolnikom ozdraviti ali lajšati njihovo stanje, milijoni ljudi po vsem svetu vsako leto trpijo zaradi nepredvidljivih toksičnih reakcij na zdravila. Zlasti pogosti so izpuščaji zaradi zdravil, ki vključujejo simptome, kot so rdečina, mehurji in srbenje kože.
Hude reakcije na zdravila so lahko smrtno nevarne in imajo dolgotrajne posledice. Zato je razumevanje, kako in zakaj se pojavijo reakcije na zdravila, pomembno področje raziskav v medicinski znanosti.
V ta namen so prejšnje študije identificirale specifične različice določenih genov kot potencialne povzročitelje izpuščajev zaradi zdravil. Znanstveniki menijo, da so pri razvoju izpuščajev zaradi zdravil vključeni geni, ki kodirajo humani levkocitni antigen (HLA), beljakovino, izraženo na površini belih krvničk, ki igra pomembno vlogo v imunskem sistemu. Vendar trenutne teorije ne morejo pojasniti, zakaj se izpuščaji zaradi zdravil, povezani s HLA, običajno pojavljajo na koži in ne v več organih po telesu.
Da bi odpravili to vrzel v znanju, je raziskovalna skupina, v kateri so bili tudi člani fakultete Shigeki Aoki, Kousei Ito in Akira Kazaoka s podiplomske šole za medicinske in farmacevtske znanosti Univerze Chiba, izvedla poglobljeno študijo o povezavi med HLA in izpuščaji zaradi zdravil. Njihove ugotovitve so bile objavljene v reviji PNAS Nexus.
Raziskovalci so najprej izvedli vrsto poskusov na mišjih keratinocitih, ki so glavna vrsta celic v koži. Te keratinocite so modificirali tako, da izražajo specifično različico gena HLA, imenovanega HLA-B57:01, ki se specifično veže na protivirusno zdravilo abakavir. Nato so te rezultate potrdili pri gensko spremenjenih miših, ki izražajo HLA-B 57:01 in so bile izpostavljene abakavirju.
Raziskovalci so ugotovili, da so keratinociti, ki izražajo HLA-B*57:01 in so bili izpostavljeni abakavirju, pokazali stresne odzive endoplazemskega retikuluma (ER), kot sta takojšnje sproščanje kalcija v citosol in povečano izražanje proteina toplotnega šoka 70 (HSP70). Opazili so tudi povečano proizvodnjo citokinov in migracijo imunskih celic. Izpostavljenost abakavirju je povzročila napačno zvijanje HLA v ER, kar je vodilo do stresa ER.
Poleg tega so raziskovalci ugotovili, da je stres endoplazmatskega retikuluma mogoče zmanjšati z uporabo 4-fenilbutirata (4-PB). Z odpravo tega stresa so lahko preprečili pojav hudih simptomov izpuščaja zaradi zdravil. To novo znanje bi lahko zagotovilo osnovo za inovativne možnosti zdravljenja izpuščajev zaradi zdravil.
Toda kako se te nove informacije razlikujejo od tistega, kar je bilo že znano o HLA?
"Molekule HLA so sestavni del našega imunskega sistema, ki običajno predstavljajo tuje antigene belim krvničkam, ki te antigene ocenijo kot lastne ali tuje. V tej uveljavljeni vlogi HLA običajno igra sekundarno vlogo," pojasnjuje dr. Aoki.
"Vendar pa naša študija poudarja novo funkcijo molekule HLA v kožnih celicah. Ugotovili smo, da lahko specifičen genotip HLA v keratinocitih prepozna določena zdravila kot tuja, kar sproži stresni odziv endoplazemskega retikuluma."
Rezultati te študije skupaj razkrivajo novo vlogo proteinov HLA pri odkrivanju in odzivanju na potencialne grožnje v kožnih celicah. Njihove funkcije tako lahko segajo daleč preko zgolj predstavitve antigenov imunskemu sistemu. Poleg tega lahko ta študija, glede na to, da je mogoče posameznikovo varianto HLA določiti z genetskim testiranjem, pomaga pri razvoju preventivnih ukrepov in diagnostičnih metod proti hudim neželenim učinkom zdravil.
Po mnenju dr. Aokija je to v skladu s trenutnimi trendi in smernicami v medicinski znanosti. »Čez 10 let pričakujemo, da bomo vstopili v dobo 'celovitega genoma', kjer bo personalizirana medicina, ki temelji na individualnih genomih, postala standardna praksa,« komentira.
"Na podlagi rezultatov te študije verjamemo, da bo celovito razumevanje mehanizma, na katerem temeljijo neželeni učinki zdravil, odvisni od HLA, omogočilo varno zdravstveno oskrbo, ki bo bolnikom omogočila, da se izognejo nepotrebnemu trpljenju zaradi stranskih učinkov."
Na splošno bi lahko prihodnje raziskave na tem področju zmanjšale pojavnost izpuščajev zaradi zdravil in ljudi rešile pred potencialno smrtnimi neželenimi učinki zdravil.
