Nove publikacije
Novi genetski mehanizmi bi lahko bili terapevtska tarča za gliom
Zadnji pregled: 02.07.2025

Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.
Študija iz laboratorija Shi-Yuan Cheng, doktorja znanosti, profesorja na oddelku za nevro-onkologijo Kena in Ruth Davey na oddelku za nevrologijo, je odkrila nove mehanizme, ki so podlaga za alternativne dogodke spajanja RNA v tumorskih celicah glioma in bi lahko služili kot nove terapevtske tarče. Rezultati študije so objavljeni v reviji Journal of Clinical Investigation.
"Našli smo drugačen način zdravljenja glioma skozi lečo alternativnega spajanja in odkrili nove tarče, ki še niso bile identificirane, vendar so pomembne za malignost glioma," je dejal Xiao Song, dr. med., izredni profesor nevrologije in glavni avtor študije.
Gliomi so najpogostejša vrsta primarnega možganskega tumorja pri odraslih in izvirajo iz glialnih celic, ki se nahajajo v osrednjem živčnem sistemu in podpirajo sosednje nevrone. Gliomi so zaradi genetske in epigenetske heterogenosti tumorja zelo odporni na standardne načine zdravljenja, vključno z obsevanjem in kemoterapijo, kar poudarja potrebo po iskanju novih terapevtskih tarč.
Prejšnje raziskave laboratorija Cheng, objavljene v reviji Cancer Research, so pokazale, da je pomemben faktor spajanja SRSF3 v gliomih bistveno povišan v primerjavi z normalnimi možgani, spajanje RNA, ki ga regulira SRSF3, pa spodbuja rast in napredovanje glioma z vplivanjem na več celičnih procesov v tumorskih celicah.
Spajanje RNK je postopek, ki vključuje odstranitev intronov (nekodirajočih regij RNK) in združitev eksonov (kodirajočih regij), da se tvori zrela molekula mRNA, ki podpira izražanje genov v celici.
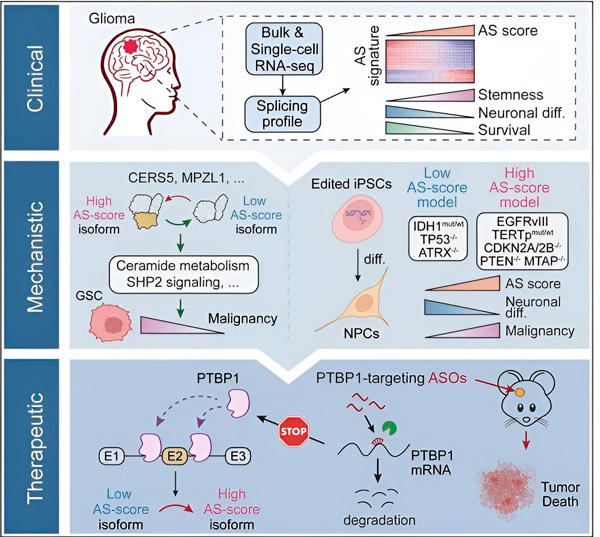
V tej študiji so znanstveniki želeli ugotoviti spremembe v alternativnem spajanju v tumorskih celicah glioma, mehanizme, na katerih temeljijo te spremembe, in določiti njihov potencial kot terapevtskih tarč.
Z uporabo računalniških metod in tehnologij sekvenciranja RNK so raziskovalci preučili spremembe spajanja v tumorskih celicah glioma iz vzorcev bolnikov. Za potrditev teh sprememb so uporabili tehnologije urejanja genov CRISPR, s katerimi so v modele glioma, pridobljene iz človeških induciranih pluripotentnih matičnih celic (iPSC), vnesli različne mutacije gonilnih genov glioma.
Ugotovili so, da te spremembe spajanja okrepi različica receptorja za epidermalni rastni faktor III (EGFRIII), za katero je znano, da je prekomerno izražena v mnogih tumorjih, vključno z gliomi, in jo zavira mutacija v genu IDH1.
Raziskovalci so potrdili funkcijo dveh dogodkov spajanja RNK, ki ustvarjata različne izooblike beljakovin z različnimi aminokislinskimi zaporedji.
"Samo ena od teh izooblik lahko spodbuja rast tumorja, v nasprotju z drugo izoobliko, ki se običajno izraža v normalnih možganih. Tumorji izkoriščajo ta mehanizem za selektivno izražanje izooblike, ki spodbuja tumor, v primerjavi z normalno izoobliko možganov," je dejal Song.
Ekipa je nato analizirala proteine, ki vežejo RNA, in ugotovila, da gen PTBP1 uravnava spajanje RNA, ki spodbuja nastanek tumorja, v celicah glioma. Z uporabo ortotopskega modela glioma pri imunsko pomanjkljivih miših so raziskovalci ciljali na PTBP1 s terapijo na osnovi antisense oligonukleotidov (ASO), kar je na koncu zavrlo rast tumorja.
"Naši podatki poudarjajo vlogo alternativnega spajanja RNA pri vplivanju na malignost in heterogenost glioma ter njegov potencial kot terapevtske ranljivosti za zdravljenje odraslih gliomov," so zapisali avtorji študije.
Naslednji korak za raziskovalce je raziskati potencial ciljanja na PTBP1 za sprožitev protitumorskega imunskega odziva, je dejal Song.
"Z analizo sekvenciranja RNK z dolgim branjem smo ugotovili, da ciljanje na PTBP1 v celicah glioma povzroči nastanek več alternativno spojenih transkriptov, ki jih v normalnih tkivih ni. Zato je naš naslednji projekt ugotoviti, ali lahko ta izoforma ustvari nekatere antigene, da lahko imunski sistem bolje prepozna tumor," je dejal Song.
Song je dodal še, da njihovo ekipo zanima analiza sprememb spajanja v netumorskih celicah bolnikov z gliomom, kot so imunske celice.
"Že vemo, da je spajanje zelo pomembno za uravnavanje delovanja v celici, zato ne bi smelo uravnavati le malignosti tumorja, temveč lahko uravnava tudi delovanje imunskih celic, da bi ugotovili, ali lahko učinkovito uničijo raka. Zato izvajamo tudi nekaj bioinformatičnih analiz v imunskih celicah, ki jih infiltrira tumor, da bi ugotovili, ali pride do spremembe v spajanju, potem ko imunska celica infiltrira tumor."
"Naš cilj je določiti vlogo alternativnega spajanja pri oblikovanju imunosupresivnega tumorskega mikrookolja in prepoznati potencialne tarče za izboljšanje učinkovitosti imunoterapij pri gliomu," je dejal Song.
