Novi dokazi izboljšujejo razumevanje vzrokov za Rettov sindrom
Zadnji pregled: 14.06.2024

Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.

Rettov sindrom je redka nevrorazvojna motnja, za katero trenutno ni zdravila ali dobre terapije. Povzroča resne telesne in kognitivne simptome, od katerih se mnogi prekrivajo z motnjami avtističnega spektra.
Rettov sindrom povzročajo mutacije v genu MECP2, ki je močno izražen v možganih in zdi se, da ima pomembno vlogo pri ohranjanju zdravja nevronov. Gen se nahaja na kromosomu X, sindrom pa prizadene predvsem dekleta. Za razvoj zdravljenja za Rettov sindrom želijo raziskovalci bolje razumeti MECP2 in njegove funkcije v možganih.
Raziskovalci, vključno s soustanoviteljem inštituta Whitehead Rudolfom Jaenischom, že desetletja preučujejo MECP2, vendar je veliko osnovnih dejstev o genu ostalo neznanih. Protein MECP2, ki ga kodira gen, sodeluje pri regulaciji genov; veže se na DNK in vpliva na ravni izražanja različnih drugih genov, kar pomeni količino beljakovin, ki jih tvorijo.
Vendar pa raziskovalci niso imeli popolnega seznama genov, na katere vpliva MECP2, in ni bilo soglasja o tem, kako MECP2 vpliva na te gene.
Zgodnje študije MECP2 so nakazovale, da gre za zaviralec, ki zmanjšuje izražanje svojih ciljnih genov, vendar so raziskave, ki so jih izvedli Jaenisch in drugi, pred tem pokazale, da MECP2 deluje tudi kot aktivator in povečuje izražanje svojih ciljnih genov – in da lahko biti najprej aktivator. Prav tako ni bil znan mehanizem delovanja MECP2 ali kaj točno protein počne, kar vodi do sprememb v izražanju genov.
Tehnološke omejitve so raziskovalcem preprečile razjasnitev teh vprašanj. Toda Yanish, podoktor v svojem laboratoriju, Yi Liu, in nekdanji član Yanishevega laboratorija, Anthony Flamier, zdaj docent na raziskovalnem središču CHU Sainte-Justine na Université de Montréal, sta uporabila najsodobnejše metode, da bi odgovorila na ta vprašanja. Preostala vprašanja o MECP2 in pridobite nove vpoglede v njegovo vlogo pri zdravju in bolezni možganov.
Njihovi rezultati so bili objavljeni v reviji Neuron, raziskovalci pa so ustvarili tudi spletno skladišče svojih podatkov MECP2, Portal MECP2-NeuroAtlas kot vir za druge raziskovalce.
"Mislim, da bo ta dokument temeljito spremenil način razmišljanja ljudi o tem, kako MECP2 povzroča Rettov sindrom. Imamo popolnoma novo razumevanje mehanizma in to lahko ponudi nove poti za razvoj zdravljenja te bolezni," pravi Jaenisch, ki je tudi profesor biologije na Massachusetts Institute of Technology.
Napredno razumevanje MECP2 v možganih
Raziskovalci so najprej ustvarili podroben zemljevid, kje se MECP2 veže v genskem zaporedju človeških nevronov, bodisi znotraj genov bodisi v regulatornih regijah DNK blizu njih. Uporabili so pristop, imenovan CUT&Tag, ki lahko z visoko natančnostjo zazna interakcije beljakovin in DNK.
Raziskovalci so odkrili več kot štiri tisoč genov, povezanih z MECP2. Ponovili so kartiranje v nevronih s pogostimi mutacijami MECP2, povezanimi z Rettovim sindromom, da bi ugotovili, kje je MECP2 izčrpan v bolezenskem stanju.
Poznavanje, na katere gene se veže MECP2, je Liuju in Flamierju omogočilo, da sta začela vzpostavljati povezave med tarčami MECP2 in zdravjem možganov. Ugotovili so, da je veliko njegovih tarč vključenih v razvoj in delovanje nevronskih aksonov in sinaps.
Primerjali so tudi svoj seznam ciljev MECP2 z zbirko podatkov Simons Foundation Autism Research Initiative (SFARI) o genih, povezanih z avtizmom, in ugotovili, da je 381 genov v tej bazi podatkov cilj MECP2.
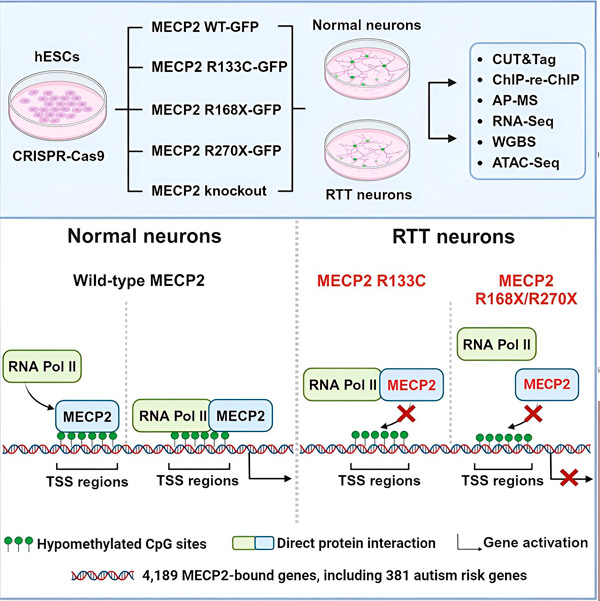
Vir: Neuron (2024). DOI: 10.1016/j.neuron.2024.04.007
Te ugotovitve lahko pomagajo razjasniti mehanizme, na katerih temeljijo simptomi avtizma pri Rettovem sindromu, in nudijo dobro izhodišče za raziskovanje možne vloge MECP2 pri avtizmu.
"Ustvarili smo prvi integriran zemljevid epigenoma MECP2 v zdravju in bolezni in ta zemljevid lahko usmerja prihodnje raziskave," pravi Liu. "Poznavanje, kateri geni so tarča MECP2 in kateri geni so neposredno moteni v bolezni, zagotavlja močno podlago za razumevanje Rettovega sindroma in postavljanje vprašanj o regulaciji genov v nevronih."
Raziskovalci so preučili tudi, ali MECP2 poveča ali zmanjša izražanje svojih ciljnih genov. V skladu z zgodovino MECP2, ki so jo nekateri opredelili kot aktivator, drugi pa kot represor, sta Liu in Flamier našla primere, kjer ima MECP2 obe vlogi.
Čeprav se MECP2 bolj pogosto obravnava kot represor, sta Liu in Flamier ugotovila, da je predvsem aktivator—potrjuje prejšnje ugotovitve Jaenisch in Liu. En nov poskus je pokazal, da MECP2 aktivira vsaj 80 % svojih tarč, drugi pa, da aktivira do 88 % svojih tarč.
Ciljni genski zemljevid, ki so ga ustvarili raziskovalci, je zagotovil dodaten vpogled v vlogo MECP2 kot aktivatorja. Ugotovili so, da se geni, ki jih aktivira MECP2, običajno vežejo na regijo DNK pred genom, imenovano mesto začetka transkripcije.
Tukaj celični stroji sprožijo proces branja gena v RNA, po katerem se RNA prevede v funkcionalno beljakovino, ki je produkt izražanja genov. Prisotnost MECP2 na mestu začetka transkripcije, kjer se začne izražanje genov, je skladna z njegovo vlogo genskega aktivatorja.
Raziskovalci so se nato odločili ugotoviti, kakšno vlogo ima MECP2 pri aktiviranju genov. Preučevali so, na katere molekule se MECP2 veže na tem mestu, poleg DNK, in ugotovili, da MECP2 neposredno sodeluje s proteinskim kompleksom, imenovanim RNA polimeraza II (RNA Pol II). RNA Pol II je ključni celični stroj, ki prepisuje DNK v RNK. RNA Pol II ne more sama najti genov, zato potrebuje veliko kofaktorjev ali sodelujočih proteinov, ki ji pomagajo opravljati svoje delo.
Raziskovalci domnevajo, da MECP2 služi kot en tak kofaktor, ki pomaga RNA Pol II sprožiti transkripcijo na genih, kjer se veže MECP2. Strukturna analiza MECP2 je identificirala dele molekule, ki se vežejo na RNA Pol II, drugi poskusi pa so potrdili, da izguba MECP2 zmanjša prisotnost RNA Pol II na ustreznih začetnih mestih transkripcije kot tudi ravni izražanja ciljnih genov.
To nakazuje, da je lahko Rettov sindrom posledica zmanjšane transkripcije genov, na katere cilja MECP2, zaradi mutacij v MECP2, ki mu preprečujejo vezavo na RNA Pol II ali na DNA. V skladu s to idejo so najpogostejše mutacije MECP2, povezane z boleznijo, okrnitve: mutacije, pri katerih manjka del proteina, kar lahko spremeni interakcijo med MECP2 in RNA Pol II.
Raziskovalci upajo, da njihove ugotovitve ne bodo samo spremenile našega razumevanja MECP2, ampak da bo globlje in širše razumevanje, kako MECP2 vpliva na razvoj in delovanje možganov, lahko vodilo do novih spoznanj, ki bodo pomagala ljudem z Rettovim sindromom in sorodnimi motnjami, vključno z avtizem.
»Ta projekt je odličen primer sodelovalne narave dela laboratorija Jaenisch,« pravi Flamier. "Rudolph in Yi sta imela posebno težavo z Rettovim sindromom, jaz pa sem imel izkušnje s tehnologijo CUT&Tag, ki bi lahko rešila to težavo. Skozi razpravo sva spoznala, da lahko združiva svoja prizadevanja in zdaj imava odlično skladišče informacij o MECP2 in njegove povezave z boleznijo."
