Sistem za dostavo zdravil z zaprto zanko bi lahko izboljšal kemoterapijo
Zadnji pregled: 14.06.2024

Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.
Ko bolniki z rakom prejemajo kemoterapijo, se odmerki večine zdravil izračunajo glede na bolnikovo telesno površino. Ta kazalnik se oceni z enačbo, v katero se nadomesti višina in teža bolnika. Ta enačba je bila oblikovana leta 1916 na podlagi podatkov le devetih bolnikov.
Ta poenostavljen pristop k odmerjanju ne upošteva drugih dejavnikov in lahko povzroči, da bolniku predpišejo preveč ali premalo zdravila. Zaradi tega lahko nekateri bolniki občutijo prekomerno toksičnost ali pomanjkanje učinkovitosti kemoterapije.
Da bi izboljšali natančnost odmerjanja kemoterapije, so inženirji MIT razvili alternativni pristop, ki omogoča prilagajanje odmerka za vsakega bolnika. Njihov sistem meri količino zdravila v pacientovem telesu, ti podatki pa se vnesejo v krmilnik, ki lahko temu primerno prilagodi hitrost infundiranja.
Ta pristop lahko pomaga nadomestiti razlike v farmakokinetiki zdravil, ki jih povzročajo telesna sestava, genetska predispozicija, toksičnost organov zaradi kemoterapije, interakcije z drugimi zdravili in hrano ter cirkadiana nihanja encimov, odgovornih za razgradnjo kemoterapevtskih zdravil, pravijo raziskovalci. p>
"Verjamemo, da lahko s prepoznavanjem napredka v razumevanju presnove zdravil in uporabo inženirskih orodij za poenostavitev prilagojenega odmerjanja pomagamo spremeniti varnost in učinkovitost številnih zdravil," pravi Giovanni Traverso, docent za strojništvo na MIT in gastroenterolog v bolnišnici. Brigham and Women's Hospital in višja avtorica študije.
Louis DeRidder, podiplomski študent MIT, je glavni avtor članka, objavljenega v Med.
Nenehno spremljanje
V tej študiji so se raziskovalci osredotočili na zdravilo, imenovano 5-fluorouracil, ki se uporablja za zdravljenje kolorektalnega raka in druge vrste raka. Zdravilo se običajno daje v 46-urnem obdobju, odmerek pa se določi s formulo, ki temelji na bolnikovi višini in teži, kar zagotavlja oceno telesne površine.
Vendar ta pristop ne upošteva razlik v telesni sestavi, ki lahko vplivajo na porazdelitev zdravila v telesu, ali genetskih variacij, ki vplivajo na njegovo presnovo. Te razlike lahko povzročijo škodljive stranske učinke, če je zdravila preveč. Če zdravilo ni dovolj, morda ne bo uničilo tumorja, kot je pričakovano.
"Ljudje z enako telesno površino imajo lahko zelo različno višino in težo, različno mišično maso ali genetiko, a dokler višina in teža, vključena v to enačbo, dajeta enako telesno površino, je njihov odmerek enak," pravi DeRidder, doktorski kandidat v programu medicinskega inženirstva in medicinske fizike na programu zdravstvenih znanosti in tehnologije Harvard-MIT.
Drugi dejavnik, ki lahko kadar koli spremeni količino zdravila v krvi, je cirkadiano nihanje encima, imenovanega dihidropirimidin dehidrogenaza (DPD), ki razgrajuje 5-fluorouracil. Izražanje DPD, tako kot mnogih drugih encimov v telesu, uravnava cirkadiani ritem. Tako razgradnja 5-FU DPD ni konstantna, ampak se spreminja glede na čas dneva. Ti cirkadiani ritmi lahko med trajanjem infuzije povzročijo desetkratna nihanja količine 5-fluorouracila v bolnikovi krvi.
"Z uporabo telesne površine za izračun odmerka kemoterapije vemo, da imata lahko dve osebi popolnoma različne toksičnosti kot 5-fluorouracil. En bolnik ima lahko cikle zdravljenja z minimalno toksičnostjo in nato cikel z grozno toksičnostjo. Nekaj se je spremenilo v tem, kako to bolnik presnavlja kemoterapijo iz enega cikla v drugega. Naša zastarela metoda odmerjanja ne zajame teh sprememb in bolniki zaradi tega trpijo,« pravi Douglas Rubinson, klinični onkolog na Inštitutu za raka Dana-Farber in avtor prispevka.
Eden od načinov za kompenzacijo variabilnosti v farmakokinetiki kemoterapije je strategija, imenovana terapevtsko spremljanje zdravil, pri kateri pacient odvzame vzorec krvi na koncu enega cikla zdravljenja. Ko je ta vzorec analiziran za koncentracije zdravila, se lahko odmerek po potrebi prilagodi na začetku naslednjega cikla (običajno po dveh tednih za 5-fluorouracil).
Izkazalo se je, da ta pristop vodi do boljših rezultatov za bolnike, vendar se ni pogosto uporabljal za kemoterapije, kot je 5-fluorouracil.
Raziskovalci MIT so želeli razviti podobno vrsto spremljanja, vendar na avtomatiziran način, ki bi lahko personaliziral odmerjanje zdravil v realnem času, kar bi lahko privedlo do boljših rezultatov za bolnike.
V njihovem sistemu z zaprto zanko je mogoče koncentracije zdravil nenehno spremljati in te informacije se uporabljajo za samodejno prilagoditev hitrosti infundiranja zdravila za kemoterapijo, da se odmerek vzdržuje znotraj ciljnega območja.
Ta sistem z zaprto zanko omogoča prilagajanje odmerjanja zdravil, da se upoštevajo cirkadiani ritmi spreminjajočih se ravni encimov, ki presnavljajo zdravila, kot tudi morebitne spremembe v farmakokinetiki bolnika od zadnjega zdravljenja, kot je toksičnost organov zaradi kemoterapije.
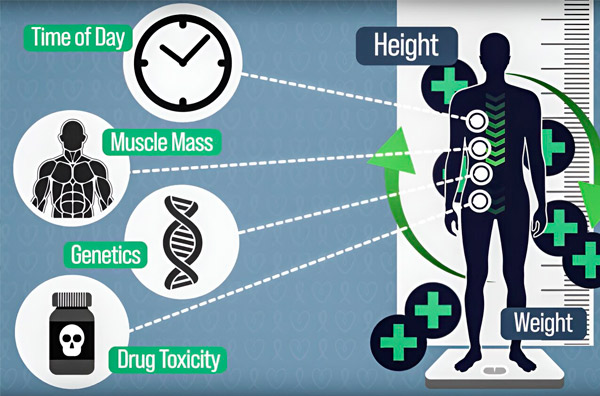
Da bi bilo odmerjanje kemoterapije natančnejše, so inženirji MIT razvili način za neprekinjeno merjenje količine zdravila v pacientovem telesu med večurno infuzijo. To bo pomagalo nadomestiti razlike, ki jih povzročajo telesna sestava, genetika, toksičnost zdravil in cirkadiana nihanja. Vir: zagotovili raziskovalci.
Novi sistem, ki so ga razvili raziskovalci, znan kot CLAUDIA (Closed-Loop Automated Drug Infusion RegulAtor), za vsak korak uporablja komercialno dostopno opremo. Vzorce krvi odvzamemo vsakih pet minut in jih hitro pripravimo za analizo. Izmerimo koncentracijo 5-fluorouracila v krvi in jo primerjamo s ciljnim območjem.
Razlika med ciljno in izmerjeno koncentracijo se vnese v kontrolni algoritem, ki nato po potrebi prilagodi hitrost infundiranja, da vzdržuje odmerek v območju koncentracije, pri kateri je zdravilo učinkovito in netoksično.
»Razvili smo sistem, v katerem lahko nenehno merimo koncentracije zdravil in ustrezno prilagodimo hitrost infundiranja, da ohranimo koncentracije zdravil znotraj terapevtskega okna,« pravi DeRidder.
Hitra prilagoditev
V poskusih na živalih so raziskovalci ugotovili, da jim je z uporabo zdravila CLAUDIA uspelo obdržati količino zdravila, ki kroži po telesu, v ciljnem območju približno 45 odstotkov časa.
Ravni zdravil pri živalih, ki so prejemale kemoterapijo brez zdravila CLAUDIA, so v povprečju ostale v ciljnem območju le 13 odstotkov časa. V tej študiji raziskovalci niso preizkušali učinkovitosti ravni zdravil, vendar se verjame, da ohranjanje koncentracij znotraj ciljnega okna povzroči boljše rezultate in manjšo toksičnost.
CLAUDIA je prav tako lahko vzdrževala odmerek 5-fluorouracila v ciljnem območju, tudi če je dajala zdravilo, ki zavira encim DPD. Pri živalih, zdravljenih s tem zaviralcem brez stalnega spremljanja in prilagajanja, so se ravni 5-fluorouracila povečale do osemkrat.
Za to predstavitev so raziskovalci ročno izvedli vsak korak postopka z uporabo standardne opreme, zdaj pa načrtujejo avtomatizacijo vsakega koraka, tako da bo mogoče spremljanje in prilagajanje odmerka izvesti brez človeškega posredovanja.
Za merjenje koncentracij zdravil so raziskovalci uporabili tekočinsko kromatografijo visoke ločljivosti z masno spektrometrijo (HPLC-MS), tehniko, ki jo je mogoče prilagoditi za odkrivanje skoraj vseh vrst zdravil.
»Predvidevamo si prihodnost, v kateri bomo lahko uporabljali CLAUDIA za katero koli zdravilo, ki ima primerne farmakokinetične lastnosti in ga je mogoče zaznati s HPLC-MS, kar omogoča prilagojeno odmerjanje za veliko različnih zdravil,« pravi DeRidder.
