Medicinski strokovnjak članka
Nove publikacije
Patogeneza hepatitisa B
Last reviewed: 07.07.2025

Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.
V patogenezi hepatitisa B je mogoče prepoznati več vodilnih členov v patogenetski verigi:
- vnos patogena - okužba;
- fiksacija na hepatocitu in prodiranje v celico;
- razmnoževanje virusa in njegovo "izrinjanje" na površino hepatocita, pa tudi v kri;
- aktivacija imunoloških reakcij, namenjenih odpravi patogena;
- poškodbe organov in sistemov z imunskimi kompleksi;
- nastanek imunosti, sprostitev patogena, okrevanje.
Ker se okužba s hepatitisom B vedno pojavi parenteralno, lahko sklepamo, da je trenutek okužbe praktično enak prodiranju virusa v kri. Poskusi nekaterih raziskovalcev, da bi razlikovali med enteralno in regionalno fazo pri hepatitisu B, so slabo utemeljeni. Več razlogov obstaja za prepričanje, da virus takoj vstopi v jetra s tokom krvi.
Tropizem virusa hepatitisa B do jetrnega tkiva je vnaprej določen s prisotnostjo posebnega receptorja v HBsAg - polipeptida z molekulsko maso 31.000 Da (P31), ki ima aktivnost vezave albuminov. Podobno albuminsko območje najdemo tudi na membrani hepatocitov v jetrih ljudi in šimpanzov, kar bistveno določa tropizem HBV do jeter ljudi in šimpanzov.
Ko virus prodre v hepatocit, se sprosti virusna DNK, ki z vstopom v jedro hepatocita in delovanjem kot matrica za sintezo nukleinskih kislin sproži vrsto zaporednih bioloških reakcij, katerih rezultat je sestavljanje virusne nukleokapside. Nukleokapsida migrira skozi jedrno membrano v citoplazmo, kjer pride do končne sestave Daneovih delcev - celotnega virusa hepatitisa B.
Vendar je treba opozoriti, da lahko pri okužbi hepatocita proces poteka na dva načina - replikativno in integrativno. V prvem primeru se razvije slika akutnega ali kroničnega hepatitisa, v drugem pa virusno prenašanje.
Razlogi, ki določajo obe vrsti interakcije med virusno DNK in hepatociti, niso natančno določeni. Najverjetneje je vrsta odziva genetsko določena.
Rezultat replikativne interakcije je sestavljanje struktur osrednjega antigena (v jedru) in sestavljanje celotnega virusa (v citoplazmi), ki mu sledi predstavitev celotnega virusa ali njegovih antigenov na membrani ali v strukturi membrane hepatocitov.
Splošno sprejeto je, da replikacija virusa ne povzroči poškodb celic na ravni hepatocitov, saj virus hepatitisa B nima citopatskega učinka. Tega stališča ni mogoče šteti za nesporno, saj temelji na eksperimentalnih podatkih, ki sicer kažejo na odsotnost citopatskega učinka virusa hepatitisa B, vendar so bili pridobljeni na tkivnih kulturah in jih zato ni mogoče v celoti ekstrapolirati na virusni hepatitis B pri ljudeh. V vsakem primeru pa vprašanje odsotnosti poškodb hepatocitov med replikacijsko fazo zahteva dodatne raziskave.
Vendar pa so ne glede na naravo interakcije virusa s celico jetra nujno vključena v imunopatološki proces. V tem primeru je poškodba hepatocitov povezana z dejstvom, da se zaradi izražanja virusnih antigenov na membrani hepatocitov in sproščanja virusnih antigenov v prosti obtok vključi veriga zaporednih celičnih in humoralnih imunskih reakcij, katerih končni cilj je odstranitev virusa iz telesa. Ta proces poteka v popolnem skladu s splošnimi vzorci imunskega odziva na virusne okužbe. Za odstranitev patogena se vključijo celične citotoksične reakcije, ki jih posredujejo različni razredi efektorskih celic: celice K, celice T, naravne ubijalke, makrofagi. Med temi reakcijami se okuženi hepatociti uničijo, kar spremlja sproščanje virusnih antigenov (HBcAg, HBeAg, HBsAg), ki sprožijo sistem za tvorbo protiteles, zaradi česar se v krvi kopičijo specifična protitelesa, predvsem proti jedru - anti-HBc in e-antigen - anti-HBE. Posledično se sproščanje jetrne celice iz virusa pojavi v procesu njene smrti zaradi reakcij celične citolize.
Hkrati se specifična protitelesa, ki se kopičijo v krvi, vežejo na virusne antigene in tvorijo imunske komplekse, ki jih makrofagi fagocitirajo in izločajo ledvice. V tem primeru se lahko pojavijo različne lezije imunskih kompleksov v obliki glomerulonefritisa, arteritisa, artralgije, kožnih izpuščajev itd. S sodelovanjem specifičnih protiteles se telo očisti patogena in pride do popolnega okrevanja.
V skladu z orisanim konceptom patogeneze hepatitisa B je vsa raznolikost kliničnih variant poteka bolezni običajno pojasnjena s posebnostmi interakcije virusa in sodelovanja imunokompetentnih celic, z drugimi besedami, z močjo imunskega odziva na prisotnost virusnih antigenov. Po sodobnih konceptih je moč imunskega odziva genetsko določena in povezana z antigeni histokompatibilnosti lokusa HLA prvega razreda.
Splošno sprejeto je, da se v pogojih ustreznega imunskega odziva na virusne antigene akutni hepatitis klinično razvije s cikličnim potekom in popolnim okrevanjem. Ob ozadju zmanjšanja imunskega odziva na virusne antigene je imunsko posredovana citoliza izražena neznatno, zato ni učinkovitega izločanja okuženih jetrnih celic, kar vodi do blagih kliničnih manifestacij z dolgotrajno perzistencijo virusa in morebiti do razvoja kroničnega hepatitisa. Hkrati pa, nasprotno, v primeru genetsko določenega močnega imunskega odziva in obsežne okužbe (hemotransfuzija) nastanejo obsežna območja poškodb jetrnih celic, ki klinično ustrezajo hudim in malignim oblikam bolezni.
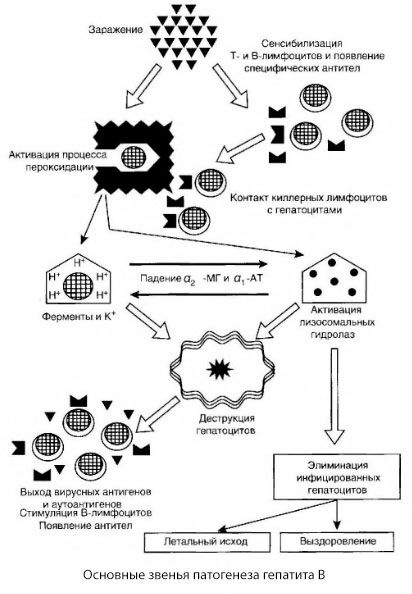
Predstavljena shema patogeneze hepatitisa B se odlikuje po svoji skladnosti, vendar vsebuje številne kontroverzne in slabo raziskane točke.
Če sledimo konceptu hepatitisa B kot imunopatološke bolezni, lahko pričakujemo povečanje celičnih citotoksičnih reakcij z naraščajočo resnostjo bolezni. Vendar pa se pri hudih oblikah indeksi celične imunosti močno zmanjšajo, vključno z večkratnim padcem v primerjavi z zdravimi otroki in indeksom citotoksičnosti K-celic. Pri maligni obliki se v obdobju razvoja masivne jetrne nekroze in zlasti jetrne kome opazi popolna nezmožnost limfocitov za blastno transformacijo pod vplivom fitohematutinina, stafilokoknega endotoksina in HBsAg. Poleg tega ni sposobnosti levkocitov za migracijo v skladu z reakcijo inhibicije migracije levkocitov (LMIC), rezultati njihovih študij z uporabo fluorescentne tetraciklinske sonde pa kažejo močno povečanje prepustnosti limfocitnih membran.
Če so torej indeksi fluorescence limfocitov pri zdravih ljudeh 9,9 ± 2 %, pri tipičnem hepatitisu B z benignim potekom pa se povečajo na 22,3 ± 2,7 %, potem pri malignih oblikah število fluorescentnih limfocitov doseže povprečno 63,5 ± 5,8 %. Ker je povečanje prepustnosti celičnih membran v literaturi nedvoumno ocenjeno kot zanesljiv pokazatelj njihove funkcionalne manjvrednosti, lahko sklepamo, da pri hepatitisu B, zlasti pri maligni obliki, pride do hude poškodbe limfocitov. To dokazujejo tudi indeksi citotoksičnosti K-celic. Pri hudi obliki je v 1. do 2. tednu bolezni citotoksičnost 15,5 ± 8,8 %, pri maligni obliki pa v 1. tednu 6,0 ± 2,6, v 2. tednu pa 22,0 ± 6,3 % z normo 44,8 ± 2,6 %.
Predstavljeni podatki jasno kažejo na izrazite motnje v celični povezavi imunosti pri bolnikih s hudimi oblikami hepatitisa B. Očitno je tudi, da se te spremembe pojavijo sekundarno, kot posledica poškodbe imunokompetentnih celic s strupenimi presnovki in morda s cirkulirajočimi imunskimi kompleksi.
Kot so pokazale študije, se pri bolnikih s hudimi oblikami hepatitisa B, zlasti v primeru razvoja masivne jetrne nekroze, titer HBsAg in HBeAg v krvnem serumu zmanjša, hkrati pa se protitelesa proti površinskemu antigenu začnejo odkrivati v visokih titrih, kar je popolnoma neznačilno za benigne oblike bolezni, pri katerih se anti-HBV pojavijo šele v 3. do 5. mesecu bolezni.
Hitro izginotje antigenov virusa hepatitisa B s hkratnim pojavom visokih titrov protivirusnih protiteles kaže na intenzivno tvorbo imunskih kompleksov in njihovo možno sodelovanje v patogenezi razvoja masivne jetrne nekroze.
Torej, dejstva nam ne omogočajo nedvoumne interpretacije hepatitisa B samo z vidika imunopatološke agresije. In bistvo ni le v tem, da ni mogoče najti povezave med globino in razširjenostjo morfoloških sprememb v jetrih na eni strani in resnostjo dejavnikov celične imunosti na drugi. Teoretično bi to okoliščino lahko pojasnili s poznimi fazami preučevanja kazalnikov celične imunosti, ko so bile imunokompetentne celice izpostavljene močnim toksičnim učinkom zaradi naraščajoče funkcionalne insuficience jeter. Seveda lahko domnevamo, da se imunska citoliza hepatocitov pojavi v najzgodnejših fazah infekcijskega procesa, morda celo pred pojavom kliničnih simptomov hude okvare jeter. Vendar je takšna predpostavka malo verjetna, saj so bili podobni kazalniki celične imunosti odkriti pri bolnikih z najakutnejšim (bliskovitim) potekom bolezni, poleg tega pa med morfološkim pregledom jetrnega tkiva ni bila odkrita masivna limfocitna infiltracija, hkrati pa so bila odkrita neprekinjena polja nekrotičnega epitelija brez pojavov resorpcije in limfocitne agresije.
Morfološko sliko akutnega hepatitisa je zelo težko razložiti le z vidika imunske celične citolize, zato v zgodnjih študijah citotoksični učinek virusa hepatitisa B ni bil izključen.
Trenutno je ta predpostavka delno potrjena z odkritjem virusa hepatitisa B. Kot so pokazale študije, je pogostost odkrivanja markerjev hepatitisa D neposredno odvisna od resnosti bolezni: pri blagih oblikah jih odkrijemo pri 14 %, pri zmernih pri 18 %, pri hudih pri 30 % in pri malignih pri 52 % bolnikov. Glede na to, da ima virus hepatitisa D nekrozogeni citopatogeni učinek, lahko štejemo za ugotovljeno, da je sočasna okužba z virusi hepatitisa B in D zelo pomembna pri razvoju fulminantnih oblik hepatitisa B.
Patogenezo hepatitisa B lahko predstavimo na naslednji način. Po prodiranju virusa hepatitisa B v hepatocite se imunološki napad na okužene hepatocite sproži s strani T-ubijalcev, ki izločajo limfotoksine v smeri jetrnih celic.
Natančni mehanizmi poškodbe hepatocitov pri hepatitisu B še niso pojasnjeni. Vodilna vloga je aktivirana lipidna peroksidacija in lizosomske hidrolaze. Sprožilec so lahko limfotoksini, ki se sproščajo iz efektorskih celic ob stiku s hepatociti, vendar je možno, da je sam virus iniciator procesov peroksidacije. Patološki proces se nato najverjetneje razvije v naslednjem zaporedju.
- Interakcija agresivnega faktorja (limfotoksinov ali virusa) z biološkimi makromolekulami (morda s komponentami membran endoplazemskega retikuluma, ki lahko sodelujejo v procesih razstrupljanja, po analogiji z drugimi škodljivimi snovmi, kot je bilo prikazano v povezavi z ogljikovim tetrakloridom).
- Nastanek prostih radikalov, aktivacija procesov lipidne peroksidacije in povečana prepustnost vseh hepatocelularnih membran (sindrom citolize).
- Gibanje biološko aktivnih snovi vzdolž koncentracijskega gradienta - izguba encimov različnih znotrajceličnih lokalizacij, donorjev energije, kalija itd. Kopičenje natrija in kalcija v celicah, premik pH proti znotrajcelični acidozi.
- Aktivacija in sproščanje lizosomskih hidrolaz (RNAze, DNAze, katepsinov itd.) z razgradnjo jetrnih celic in sproščanjem avtoantigenov.
- Stimulacija T- in B-imunskih sistemov z nastankom specifične senzibilizacije T-limfocitov na jetrne lipoproteine, kot tudi nastajanje antihepatičnih humoralnih avtoprotiteles.
V predlagani shemi patogeneze hepatitisa B je sprožilni dejavnik virusni antigeni, katerih intenzivna proizvodnja se opazi v najzgodnejših fazah bolezni in skozi celotno akutno obdobje, z izjemo malignih oblik, pri katerih proizvodnja virusnih antigenov praktično preneha v času razvoja masivne jetrne nekroze, kar vnaprej določa hitro zmanjšanje virusne replikacije.
Očitno je tudi, da virusni antigeni aktivirajo T- in B-sistem imunosti. Med tem procesom pride do značilne prerazporeditve subpopulacij T-limfocitov, katere cilj je organizirati ustrezen imunski odziv, izločiti okužene hepatocite, nevtralizirati virusne antigene, sanogenezo in okrevati.
Ko imunokompetentne celice interagirajo z virusnimi antigeni na membranah hepatocitov ali med razmnoževanjem virusa znotraj hepatocita, nastanejo pogoji za aktivacijo procesov lipidne peroksidacije, ki, kot je znano, nadzoruje prepustnost vseh celičnih in subceličnih membran.
S tega vidika postane razumljiv pojav sindroma citolize, povečane prepustnosti celičnih membran, ki je tako naravna in zelo značilna za virusni hepatitis.
Končni izid sindroma citolize je lahko popolna prekinitev oksidativne fosforilacije, uhajanje celičnega materiala in smrt jetrnega parenhima.
Vendar pa v veliki večini primerov ti procesi ne dobijo tako usodnega razvoja. Le pri malignih oblikah bolezni patološki proces poteka plazovit in nepovratno, saj pride do masivne okužbe, izrazitega imunskega procesa, prekomerne aktivacije peroksidacijskih procesov in lizosomskih hidrodaz ter pojavov avtoimunske agresije.
Isti mehanizmi so opaženi pri ugodnem poteku hepatitisa B, z edino posebnostjo, da se vsi uresničujejo na kvalitativno drugačni ravni. Za razliko od primerov masivne jetrne nekroze je pri ugodnem poteku bolezni število okuženih hepatocitov in s tem območje imunopatološke citolize manjše, procesi lipidne peroksidacije niso tako bistveno okrepljeni, aktivacija kislih hidrolaz vodi le do omejene avtolize z neznatnim sproščanjem avtoantigenov in zato brez masivne avtoagresije, torej vse faze patogeneze pri ugodnem poteku potekajo v okviru ohranjene strukturne organizacije jetrnega parenhima in so omejene z obrambnimi sistemi (antioksidanti, inhibitorji itd.) in zato nimajo tako uničujočega učinka.
Vzroki za simptome zastrupitve pri virusnem hepatitisu niso bili v celoti raziskani. Predlog o razlikovanju med tako imenovano primarno ali virusno zastrupitvijo in sekundarno (izmenjalno ali presnovno) se lahko šteje za pozitivnega, čeprav to ne razkriva intimnega mehanizma nastanka splošnega toksičnega sindroma. Prvič, virusi hepatitisa nimajo toksičnih lastnosti, in drugič, koncentracija mnogih presnovkov ni vedno v korelaciji z resnostjo bolezni in stopnjo izražanja simptomov toksikoze. Znano je tudi, da koncentracija virusnih antigenov ni strogo povezana z resnostjo zastrupitve. Nasprotno, z naraščajočo resnostjo bolezni in s tem s povečanjem stopnje toksikoze se koncentracija HBsAg zmanjšuje in je najnižja pri malignih oblikah ob nastopu globoke jetrne kome. Hkrati sta pogostost odkrivanja in titri specifičnih protivirusnih protiteles neposredno odvisni od resnosti bolezni.
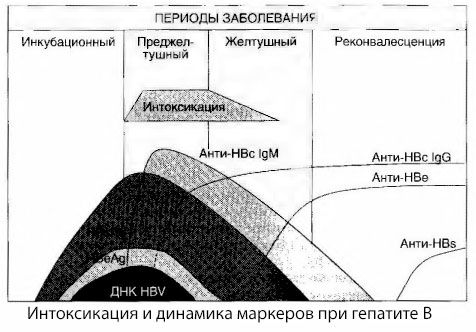
Zastrupitev se ne pojavi v trenutku registracije virusnih antigenov, temveč v obdobju kroženja v krvi protivirusnih protiteles razreda IgM proti kravjemu antigenu in antigenu sistema E. Poleg tega ima pri hudih in zlasti malignih oblikah znaten delež bolnikov v krvi celo anti-HBs, kar pri blagih in zmernih oblikah bolezni običajno nikoli ne opazimo.
Predstavljeni podatki nam omogočajo sklepati, da sindrom toksikoze pri virusnem hepatitisu, zlasti pri hepatitisu B, ne nastane kot posledica pojava virusnih antigenov v krvi, temveč je posledica interakcije virusnih antigenov z protivirusnimi protitelesi razreda IgM. Rezultat takšne interakcije je, kot je znano, nastanek imunskih kompleksov in morda aktivnih strupenih snovi.
Simptomi zastrupitve se pojavijo v trenutku pojava imunskih kompleksov v prostem obtoku, vendar se takšna korelacija pozneje ne opazi.
Delno razlago za to lahko najdemo v preučevanju sestave imunskih kompleksov. Pri bolnikih s hudimi oblikami v krvi krožijo pretežno srednje veliki kompleksi, v njihovi sestavi pa na vrhuncu toksičnega sindroma prevladujejo protitelesa razreda, medtem ko v obdobju upadanja kliničnih manifestacij in okrevanja kompleksi postanejo večji, v njihovi sestavi pa začnejo prevladovati protitelesa razreda IgG.
Predstavljeni podatki se nanašajo na mehanizme razvoja toksičnega sindroma v začetnem obdobju bolezni, vendar imajo pri toksikozi, ki se pojavi na vrhuncu kliničnih manifestacij, le delni pomen, zlasti pri razvoju jetrne kome.
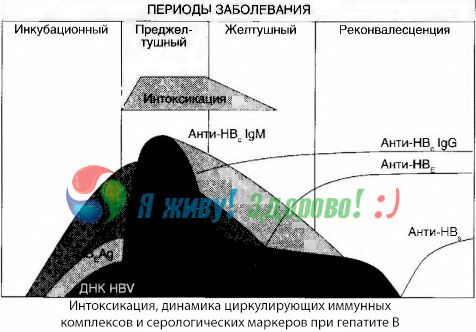
Metoda krvnih kultur je pokazala, da se pri hepatitisu B toksini nenehno kopičijo v krvi, ki se sproščajo iz poškodovanega, razpadajočega jetrnega tkiva. Koncentracija teh toksinov je sorazmerna z resnostjo bolezni, so beljakovinske narave.
Med obdobjem okrevanja se v krvi pojavijo protitelesa proti temu toksinu; v primeru jetrne kome pa se koncentracija toksina v krvi močno poveča in protiteles v krvi ne zaznamo.
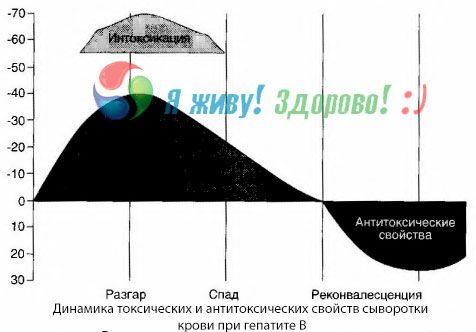
Patomorfologija hepatitisa B
Glede na naravo morfoloških sprememb ločimo tri oblike akutnega hepatitisa B:
- ciklična oblika,
- obsežna nekroza jeter;
- holestatski periholangiolitični hepatitis.
Pri ciklični obliki hepatitisa B so distrofične, vnetne in proliferativne spremembe bolj izrazite v središču lobulov, medtem ko so pri hepatitisu A lokalizirane vzdolž oboda lobula in se širijo proti središču. Te razlike so razložene z različnimi potmi prodiranja virusa v jetrni parenhim. Virus hepatitisa A vstopi v jetra skozi portalno veno in se razširi v središče lobulov, virus hepatitisa B pa prodre skozi jetrno arterijo in kapilarne veje, ki enakomerno oskrbujejo vse lobule, vse do njihovega središča.
Stopnja poškodbe jetrnega parenhima v večini primerov ustreza resnosti kliničnih manifestacij bolezni. Pri blagih oblikah običajno opazimo fokalno nekrozo hepatocitov, pri zmernih in hudih oblikah pa zonsko nekrozo (z nagnjenostjo k združevanju in tvorbi mostičaste nekroze pri hudih oblikah bolezni).
Največje morfološke spremembe v parenhimu opazimo na vrhuncu kliničnih manifestacij, kar običajno sovpada s prvim desetletjem bolezni. V drugem in zlasti tretjem desetletju se regeneracijski procesi okrepijo. V tem obdobju nekrobiotične spremembe skoraj popolnoma izginejo in prevladujejo procesi celične infiltracije s počasno nadaljnjo obnovo strukture hepatocelularnih plošč. Vendar pa se popolna obnova strukture in funkcije jetrnega parenhima pojavi šele 3-6 mesecev po začetku bolezni in ne pri vseh bolnikih.
Generalizirano naravo okužbe pri hepatitisu B potrjuje odkrivanje HBsAg ne le v hepatocitih, temveč tudi v ledvicah, pljučih, vranici, trebušni slinavki, celicah kostnega mozga itd.
Holestatični (periholangiolitični) hepatitis je posebna oblika bolezni, pri kateri se največje morfološke spremembe pojavijo na strani intrahepatičnih žolčnih vodov, s sliko holangiolitisa in periholangiolitisa. Pri holestatični obliki se holestaza pojavi z razširitvijo žolčnih kapilar s stazo žolča v njih, s proliferacijo holangiole in celičnimi infiltrati okoli nje. Jetrne celice so pri tej obliki hepatitisa neznatno prizadete. Klinično je za bolezen značilen dolgotrajen potek s podaljšano zlatenico. Dokazano je, da je vzrok za tako svojevrsten potek bolezni prevladujoč učinek virusa na stene holangiole z neznatnim učinkom na hepatocite.

