Medicinski strokovnjak članka
Nove publikacije
Restenoza
Last reviewed: 04.07.2025

Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.
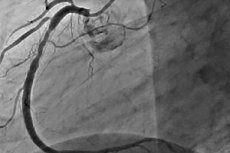
Restenoza je razvoj ponavljajoče se zožitve za 50 % ali več na mestu perkutane koronarne intervencije. Restenozo običajno spremlja ponavljajoča se angina pektoris, ki pogosto zahteva ponavljajoče se intervencije. Z razvojem perkutane koronarne intervencije se je incidenca restenoze zmanjšala, spremenila pa se je tudi njena narava.
Restenoza po transluminalni balonski koronarni angioplastiki (TBCA)
Po TBCA je stopnja restenoze v prvih 6 mesecih 30–40 %. Glavni mehanizem njenega razvoja je lokalno negativno preoblikovanje žile, ki je v bistvu elastični kolaps arterijskega lumna, ki ga balon med postopkom razširi. Lokalna tvorba tromba in rast neointimale prav tako igrata relativno vlogo. Obstajajo klinični (sladkorna bolezen tipa 2, akutni koronarni sindrom (AKS), anamneza restenoze), angiografski (lezija LAD, majhen premer žile, kronična popolna okluzija (KTO), dolga lezija, degenerirani venski bypass presadki) in proceduralni (velika rezidualna stenoza, majhno povečanje premera žile kot posledica napihovanja balona) dejavniki tveganja za restenozo po TBCA. V primeru restenoze se običajno izvede ponovni poseg. Uspeh ponovne TBCA na mestu restenoze je primerljiv s prvim posegom. Vendar pa se z vsako naslednjo TBCA zaradi restenoze tveganje za ponovitev restenoze znatno poveča. Po 3. poskusu doseže 50–53 %. Poleg tega je pri vsaki ponovitvi TBCA razvijajoča se restenoza bolj izrazita kot prva. Dejavniki tveganja za restenozo po drugi TBCA zaradi restenoze so zgodnji pojav prve restenoze (60–90 dni po posegu), poškodba LAD, poškodba več žil, sladkorna bolezen tipa 2, arterijska hipertenzija, nestabilna angina pektoris in večkratno napihovanje balonov med prvim posegom. Glede na visoko pogostost restenoze in mehanizem njenega razvoja so bili v klinično prakso uvedeni koronarni stenti, ki bi teoretično morali odpraviti negativno preoblikovanje žil po TBCA.
Prvi študiji, ki sta dokazali učinkovitost stentiranja, sta bili študiji STRESS in BENESTENT, objavljeni leta 1993. V študijo BENESTENT je bilo vključenih 516 bolnikov z novo diagnosticirano stenozo koronarnih arterij s premerom več kot 3 mm, ki so bili naključno razdeljeni v dve skupini: konvencionalna TBCA (n = 257) in TBCA z namestitvijo stenta (n = 259). Po 3 letih je bila stopnja restenoze med angiografijo 32 % v skupini s konvencionalno TBCA in 22 % v skupini s stentiranjem. Relativno zmanjšanje stopnje restenoze je bilo 31 % (p < 0,01). Skupina s stentiranjem je imela tudi manjšo potrebo po ponovni revaskularizaciji miokarda (10 v primerjavi z 20,6 % v skupini s konvencionalno TBCA; p < 0,01), kar je bilo povezano z manjšo stopnjo ponovitve angine pektoris v skupini s stentiranjem.
Glede na študijo STRESS (n = 407) je bila stopnja restenoze v skupini s stentiranjem (n ~ 205) prav tako nižja kot v skupini s konvencionalno PTCA (n = 202) - 31,6 v primerjavi s 42,1 % (p < 0,01). Prednost uporabe stentov pred konvencionalno angioplastiko v primeru restenoze na mestu PTCA je bila dokazana v študiji REST, v kateri je bilo 383 bolnikov z restenozo naključno razporejenih v skupino s stentiranjem ali ponovno perkutano transluminalno koronarno angioplastiko. Angiografsko odkrita ponovna restenoza je bila v skupini s stentiranjem za 18 % manjša (18 v primerjavi s 5,32 %; p < 0,03). Ponavljajoča se miokardna revaskularizacija, ki je pokazatelj klinično pomembne restenoze, je bila v skupini bolnikov, ki so jim vstavili stent, potrebna tudi bistveno manj pogosto (10 v primerjavi s 27 %; p < 0,001). Tako so bili boljši rezultati z uporabo stentiranja dokazani ne le v nativnih arterijah, temveč tudi v primeru intervencije zaradi restenoze, ki se je razvila po TBCA.
Restenoza po implantaciji golega stenta (BSI)
Čeprav so odkriti koronarni stenti zmanjšali incidenco restenoze za 30–40 % v primerjavi s TBCA, se pri 17–32 % bolnikov razvije restenoza v stentu tudi po stentiranju, kar zahteva ponovno revaskularizacijo. Mehanizem razvoja stenoze v stentu (ISS) se razlikuje od mehanizma pri TBCA. Po stentiranju k restenozi prispeva predvsem nastanek neointime in ne negativno preoblikovanje, kot pri TBCA, ki ga na mestu vstavitve stenta praktično ni. Neointima nastane z migracijo in proliferacijo gladkih mišičnih celic, ki tvorijo zunajcelični matriks, ki skupaj s celicami tvori neointimo. Poleg tega je pri bolnikih s sladkorno boleznijo pomembna tudi perzistencija tromba na mestu vstavitve stenta.
Glavna klasifikacija stenoze v stentu (ISS) je klasifikacija, ki jo je predlagal Mehran, ki vključuje štiri tipe, odvisno od obsega in resnosti lezije: I tip ISS - lokalna (dolžina < 10 mm), II tip - difuzna (dolžina > 10 mm), III tip - proliferativna (> 10 mm in sega čez stent) in IV tip - ISS, ki vodi do okluzije. Prvi tip je razdeljen na podtipe glede na lokacijo v stentu: 1a - na ovinku ali med stenti, 1b - marginalna, 1c - znotraj stenta, 1d - multifokalna.
Dejavniki tveganja za razvoj VRS so posegi na venskih bypass presadkih, kronične okluzije, ostialne lezije, majhen premer žil, prisotnost rezidualne stenoze, stentiranje za VRS, majhen premer žil po posegu, lezija LAD, dolga dolžina stenta, prisotnost sladkorne bolezni, implantacija več stentov v eno lezijo. Obstajajo indikacije o vplivu genetskih dejavnikov, zlasti polimorfizma gena za glikoprotein IIIa in mutacij gena za metilentetrahidrofolat reduktazo - gena, ki kodira interlevkin-1. V primeru razvoja marginalne restenoze stenta je glavni dejavnik tveganja izrazita aterosklerotična lezija v stentiranem segmentu.
Restenoza se pojavlja pretežno v prvih 6-8 mesecih po perkutani koronarni intervenciji. Večina bolnikov razvije klinične simptome približno v istem času. VRS se običajno kaže s ponavljajočo se angino pektoris. Nestabilna angina pektoris se pojavlja manj pogosto (11-41 % primerov). Akutni miokardni infarkt se razvije pri 1-6 % bolnikov. Tako je najpogostejši vzrok angine pektoris v obdobju 1-6 mesecev po stentiranju razvoj VRS, ki praviloma zahteva ponavljajočo se revaskularizacijo. Obstaja več metod za zdravljenje VRS. Izvede se lahko konvencionalna TBCA, ki vodi do nadaljnje širitve stenta (56 % prispevek h končnemu povečanju premera žile) in potisne neointimo skozi celice stenta (44 % prispevek h končnemu povečanju premera). Vendar pa se v večini primerov na mestu posega opazi preostala restenoza (v povprečju 18 %). Poleg tega je po TBCA v 11 % primerov potrebna ponovna revaskularizacija, pogosteje pri bolnikih z večžilno boleznijo, nizkim LVEF, v primeru posegov na venskih bypass presadkih ali zgodnjega pojava prvega VRS. Tveganje za razvoj ponovnega VRS po TBCA je odvisno tudi od vrste lezije in se giblje od 10 % v primeru lokalne restenoze do 80 % v primeru okluzije znotraj stenta. Vsaditev LES na mesto VRS ne zmanjša tveganja za njegovo ponovitev v primerjavi s samo TBCA.
Druga metoda zdravljenja VRS je brahiterapija, pri kateri se v lumen koronarne arterije vnese radioaktivni vir, kar prepreči proliferacijo gladkomišičnih celic in s tem zmanjša tveganje za restenozo. Vendar pa so visoki stroški opreme, tehnična zahtevnost postopka in povečana incidenca pozne tromboze stenta (LT) brahiterapijo skoraj popolnoma izključili iz klinične uporabe.
Revolucionaren trenutek pri zdravljenju VRS je bila uvedba stentov, ki sproščajo zdravilo. V primerjavi z LES v nativnih arterijah zmanjšajo tveganje za VRS za 70–80 %. Prvi podatki o učinkovitosti DES pri bolnikih z že razvitim VRS so bili pridobljeni v registru bolnikov TAXUS III, v katerem je bila pri uporabi SPG1 pri takšnih bolnikih pogostost ponovitve VRS po 6 mesecih le 16 %, kar je manj kot v prej omenjenih študijah s TBCA. V registru TRUE, ki je vključeval bolnike po implantaciji SES zaradi restenoze LES, je bila po 9 mesecih ponovna revaskularizacija potrebna pri manj kot 5 % bolnikov, predvsem s sladkorno boleznijo in AKS. Študija TROPICAL je primerjala pogostost ponovne restenoze pri bolnikih po implantaciji DES na mestu restenoze s podatki študij GAMMA I in GAMMA II, v katerih je bila kot metoda zdravljenja uporabljena brahiterapija. Po 6 mesecih je bila incidenca ponovitve restenoze v skupini SPS bistveno nižja (9,7 v primerjavi s 40,3 %; p < 0,0001). Pomembno je omeniti, da je bila incidenca tromboze stenta in miokardnega infarkta prav tako nižja v skupini SPS (TS 0,6 v primerjavi s 3,9 %; p = 0,08; MI - 1,8 v primerjavi z 9,4 %; p = 0,004). Prednost SPS pred brahiterapijo je bila potrjena v randomizirani študiji SISR, v kateri je bilo 384 bolnikov z razvitim VRS v NSC naključno razporejenih v skupino z brahiterapijo ali implantacijo SPS. Po 9 mesecih je bila potreba po ponovni revaskularizaciji po brahiterapiji večja (19,2 %) kot v skupini z implantacijo SPS (8,5 %), kar je odražalo pogostejšo ponovitev restenoze. Po 3 letih je prednost SPS v smislu zmanjšanja potrebe po ponovni revaskularizaciji zaradi ponavljajoče se restenoze stenta ostala (19 v primerjavi z 28,4 %). Med skupinama ni bilo pomembne razlike v incidenci tromboze.
Glavni dejavniki za razvoj ponavljajoče se restenoze VRS pri bolnikih z LES v primeru implantacije SPS so majhen premer žile (< 2,5 mm), difuzni tip restenoze in prisotnost kronične ledvične odpovedi, ki zahteva hemodializo. V randomizirani študiji TAXUS V ISR je SPS prav tako pokazal visoko učinkovitost pri zdravljenju VRS, saj je zmanjšal stopnjo ponavljajoče se restenoze za 54 % v primerjavi z brahiterapijo.
Izvedene so bile tudi randomizirane študije, ki so primerjale učinkovitost TBCA pri implantaciji VRS in DES. V randomizirani študiji RIBS-II je bila po 9 mesecih ponovna restenoza po implantaciji DES za 72 % manj pogosta kot po TBCA, kar je zmanjšalo potrebo po ponovni revaskularizaciji s 30 na 11 %. Študija ISAR DESIRE je primerjala učinkovitost TBCA za VRS z implantacijo SPP ali SPS. Po 6 mesecih se je izkazalo, da sta bila oba DES učinkovitejša pri preprečevanju ponovne restenoze kot TBCA (njena incidenca je bila 44,6 % pri TBCA, 14,3 % v skupini SPS in 21,7 % v skupini SPS), kar je zmanjšalo potrebo po ponovni revaskularizaciji. V neposredni primerjavi SPP in SPS je bilo ugotovljeno, da SPS bistveno učinkoviteje zmanjša potrebo po ponovni revaskularizaciji kot SPP (8 v primerjavi z 19 %). Tako implantacija DES zmanjša incidenco ponavljajočih se LES VRS v primerjavi s TBCA in brahiterapijo, kar zmanjša število ponovitev PCI in zato postane njihova implantacija postopek izbire pri takih bolnikih.
Restenoza po implantaciji stenta, ki sprošča zdravilo (DES)
Kljub 70–80-odstotnemu zmanjšanju incidence stenoze v stentu pri uporabi DES v primerjavi z LES niso mogli popolnoma izključiti razvoja te jatrogene posledice stentiranja. Njena skupna incidenca ostaja v povprečju manjša od 10 %. Poleg kvantitativnega zmanjšanja incidence restenoze so pomembno spremenili tudi vrsto restenoze, ki se pojavi. Tako je po implantaciji DES restenoza običajno fokalna. Klinično se, tako kot pri LES, najpogosteje kaže kot recidiv stabilne angine pektoris (77 %), redkeje (8 %) je asimptomatska. V 5 % primerov se kaže kot nestabilna angina pektoris, v 10 % pa je njen prvi simptom miokardni infarkt brez zobca Q. Glavni dejavniki pri razvoju restenoze pri DES so sladkorna bolezen tipa 2, majhen premer žile in obseg lezije. Za zdravljenje takšnih bolnikov ni jasnih priporočil. Alternativne možnosti so ponovna implantacija DES (iste ali drugačne vrste), TBCA ali brahiterapija. Povprečna stopnja ponovne restenoze z drugim DES je 24 % in je enaka, ne glede na to, ali je vsajen isti tip DES ali drug.


 [
[