Medicinski strokovnjak članka
Nove publikacije
Osteoartritis: vpliv menisksektomije na sklepni hrustanec
Last reviewed: 04.07.2025

Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.
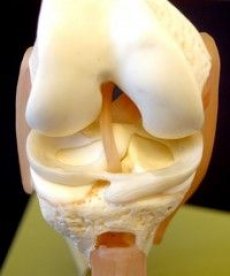
Kot smo že omenili, imajo sklepni meniskusi pomembno vlogo pri normalnem delovanju sklepov. Meniskusi so strukture, ki povečajo skladnost sklepnih površin stegnenice in golenice, izboljšajo lateralno stabilnost ter izboljšajo porazdelitev sinovialne tekočine in izmenjavo hranil s sklepnim hrustancem. Popolna ali delna meniscektomija povzroči spremembo smeri obremenitve na sklepni površini golenice, kar povzroči degeneracijo sklepnega hrustanca.
Številne študije so bile posvečene preučevanju vpliva meniscektomije na biomehaniko sklepa, pa tudi indukciji degenerativnih procesov v sklepnem hrustancu in subhondralni kosti pri živalih (običajno psih in ovcah). Sprva so raziskovalci izvedli ektomijo medialnega meniskusa kolenskega sklepa, kasneje pa so ugotovili, da ektomija lateralnega meniskusa vodi do hitrejšega razvoja osteoartritisa.
Little in sodelavci (1997) so z lateralno meniscektomijo pri ovcah preučevali spremembe v sklepnem hrustancu in subhondralni kosti na več področjih kolenskega sklepa. Tipične histološke ugotovitve, ki ponazarjajo povzročene spremembe v sklepnem hrustancu 6 mesecev po operaciji, so bile cepanje hrustanca, zmanjšana koncentracija proteoglikanov in zmanjšano število hondrocitov. Pod območji spremenjenega hrustanca v subhondralni kosti so opazili rast kapilar v kalcificirano hrustančno območje, premik "valovitega roba" navzven in odebelitev gobaste snovi subhondralne kosti.
V študiji P. Ghosha in sodelavcev (1998) je bilo dokazano, da so 9 mesecev po lateralni meniscektomiji pri ovcah prisotni znaki subhondralne preobrazbe kosti in povečanje njene mineralne gostote zaradi degeneracije sklepnega hrustanca. Na območjih, ki so izpostavljena nenormalno visoki mehanski obremenitvi zaradi odstranitve lateralnega meniskusa (lateralni kondil stegnenice in lateralna plošča golenice), je bila ugotovljena povečana sinteza proteoglikanov, ki vsebujejo dermatan sulfat, čeprav je bila povečana sinteza proteoglikanov iste vrste ugotovljena tudi v hrustancu medialne plošče. Izkazalo se je, da proteoglikane, ki vsebujejo dermatan sulfat, predstavlja predvsem dekorin. Njegova najvišja koncentracija je bila najdena v srednjih in globokih conah sklepnega hrustanca.
Poleg povečane sinteze proteoglikanov, ki vsebujejo dermatan sulfat, na obremenjenih območjih hrustanca zaradi odstranitve lateralnega meniskusa so zaznali tudi povečan katabolizem agrekana, kar dokazuje sproščanje njegovih fragmentov v hranilni medij iz hrustančnih eksplantatov, ter visoko aktivnost MMP in agrekanaz. Ker je bila vnetna aktivnost v tem modelu osteoartroze minimalna, so avtorji predlagali, da so vir encimov hondrociti.
Čeprav ostaja veliko neodgovorjenih vprašanj, zgoraj opisane študije razkrivajo možno vlogo biomehanskih dejavnikov pri patogenezi osteoartritisa. Jasno je, da so hondrociti sposobni "zaznati" mehanske lastnosti svojega okolja in se na spremembe odzvati s sintezo zunajcelične mase (ECM), ki lahko prenese večje obremenitve in tako prepreči poškodbe hrustanca. Pri mladih živalih je zmerna vadba povzročila sintezo ECM, bogatega z agrekani. Ta hipertrofična (ali prilagoditvena) faza odziva hondrocitov lahko traja več let in zagotavlja stabilno raven mehanske obremenitve sklepnega hrustanca. Vendar pa lahko motenje tega ravnovesja zaradi povečane intenzivnosti ali trajanja obremenitve ali sprememb v normalni biomehaniki sklepov po poškodbi ali operaciji ali zmanjšanja sposobnosti hondrocitov, da povečajo sintezo ECM kot odziv na povečano obremenitev (med staranjem), povzroči delovanje endokrinih dejavnikov pomembne spremembe na celični in matriksni ravni: zavira se sinteza proteoglikanov in kolagena tipa II, spodbuja pa se sinteza dekorina in kolagena tipov I, III in X. Hkrati s spremembo biosinteze se poveča katabolizem zunajceličnega matriksa (ECM), pa tudi raven MMP in agrekanaz. Ni znano, kako mehanska obremenitev spodbuja resorpcijo okoliškega ECM s strani hondrocitov; ta proces verjetno posredujejo prostanoidi, citokini (kot sta IL-1p ali TNF-a) in prosti kisikovi radikali. Tukaj je treba omeniti vlogo sinovitisa pri osteoartritisu, saj so najverjetnejši vir zgoraj omenjenih mediatorjev katabolizma lahko makrofagom podobni sinovociti in levkociti, ki infiltrirajo sinovialno membrano sklepa.
Študija OD Chrismana in sodelavcev (1981) je pokazala, da travmatska poškodba sklepa spodbuja nastajanje predhodnika prostaglandinov, arahidonske kisline. Membrane poškodovanih hondrocitov veljajo za vir arahidonske kisline. Dobro je znano, da se arahidonska kislina hitro pretvori v prostaglandine z encimom ciklooksigenaza (COX). Dokazano je, da prostaglandini, zlasti PGE2 , interagirajo s hondrocitnimi receptorji in spreminjajo izražanje njihovih genov. Vendar pa ostaja nejasno, ali arahidonska kislina spodbuja ali zavira nastajanje proteinaz in agrekanaz. Prejšnje študije so pokazale, da PGE2 poveča nastajanje MMP in povzroči razgradnjo sklepnega hrustanca. Glede na rezultate drugih študij ima PGE2 anabolični učinek na zunajcelični matrični ovoj (ECM) in spodbuja tudi integriteto ECM, saj zavira nastajanje citokinov s strani hondrocitov. Možno je, da so nasprotujoče si ugotovitve teh študij posledica različnih koncentracij PGE2, ki so bile uporabljene v njih.
Kot odziv na poškodbo sklepnega hrustanca se lahko tvori majhna količina IL-1β (glavnega citokina, ki spodbuja sintezo in sproščanje MMP ter zavira aktivnost njihovih naravnih inhibitorjev), kar vodi v nadaljnjo razgradnjo tkiva.
Študije, opisane v tem razdelku, so tako pokazale, da vzdrževanje podpragovne dinamične obremenitve sklepa povzroča proliferacijo hondrocitov, ki so sposobni prenesti nove mehanske pogoje, kar pomeni začetek hipertrofične faze osteoartroze. Hipertrofirani hondrociti so celice v zadnji fazi diferenciacije, kar pomeni, da je v njih spremenjena ekspresija genov glavnih elementov matriksa. Zato je zavirana sinteza agrekanskih proteoglikanov in kolagena tipa II, povečana pa je sinteza dekorina, kolagenov tipa I, III in X.
Zmanjšanje vsebnosti agrekana in kolagena tipa II v zunajceličnem materničnem telesu (ECM), povezano z neravnovesjem med procesi sinteze in razgradnje, daje sklepnemu hrustancu lastnost neustreznega odzivanja na mehanske obremenitve. Posledično hondrociti postanejo nezaščiteni, proces pa preide v tretjo, katabolno fazo, za katero je značilna prekomerna proteolitična aktivnost in izločanje avtokrinih in parakrinih regulatornih dejavnikov. Morfološko je ta faza značilna po uničenju zunajcelične materničnega telesa sklepnega hrustanca; klinično ustreza manifestni osteoartrozi. Ta hipoteza seveda predstavlja poenostavljen pogled na vse kompleksne procese, ki se pojavljajo pri osteoartrozi, vendar posplošuje sodoben koncept patobiologije osteoartroze.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]

