Medicinski strokovnjak članka
Nove publikacije
Restenoza
Zadnji pregled: 23.04.2024

Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.
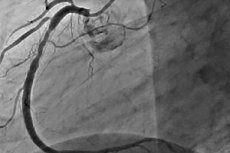
Restenoza je razvoj ponavljajočega zoženja 50% ali več na mestu perkutane koronarne intervencije. Restenozo ponavadi spremlja ponovitev angine, kar pogosto zahteva ponavljajoče posege. Ker se je PCI razvil, se je pojavnost restenoze zmanjšala, poleg tega pa se je spremenil tudi njegov značaj.
Restenoza po translumalni balonski koronarni angioplastiki (TBA)
Po izvedbi TBA je bila incidenca restenoze v prvih 6 mesecih. Je 30-40%. Glavni mehanizem njegovega razvoja je lokalna negativen preoblikovanje plovila, ki je vendar Pravzaprav, je elastični spadenie lumen arterije, balon razširila med postopkom. Relativno vlogo ima tudi lokalna tromboza in neointimalna rast. Dodeli klinično (diabetes mellitus tipa 2, akutni koronarni sindrom (AKS), zgodovina restenoze), angiografijo (fant lezije, plovilo majhnega premera, kronične popolno okluzijo (hto), globoko lezije, degenerirana vene cepičev) in čiščenje (visoka preostalo stenoza, majhno povečanje premera plovila zaradi inflacije balona) dejavniki tveganja za restenozo po TBA. V primeru restenoze se praviloma izvaja ponavljajoče poseganje. Uspeh ponavljajoče se TBA v kraju restenoze je primerljiv s prvim postopkom. Toda z vsakim nadaljnjim TBCA za restenozo se tveganje ponovitve restenoze znatno poveča. Po tretjem poskusu doseže 50 -53%. Poleg tega je pri vsakem ponavljajočem se TBA razvijanje restenoze bolj izrazito kot prvo. Dejavniki tveganja za razvoj restenoze po drugi TBCA za restenoze so zgodnji pojav prvega restenoze (60-90 dni po posegu), PNA poraz mnogososudistos lezija, prisotnost sladkorne bolezni tipa 2, povišan krvni tlak, nestabilna angina pektoris, kot tudi večkratno inflacije balon na prvi postopek. Glede na visoko incidenco restenoze, in mehanizem za njen razvoj v klinični praksi so bile uvedene koronarnih žilnih opornic, ki bi morali teoretično odpraviti negativne vaskularno preoblikovanje po TBCA.
Prve študije, ki so pokazale učinkovitost uporabe stentov, so bile objavljene leta 1993, študije STRESS in BENESTENT. V BENESTENT vključen 516 bolnikov z novo diagnosticiranim stenoze v koronarnih arterijah s premerom večji od 3 mm, ki so naključno razdelili v dve skupini: Redni TBCA (n = 257) TBCA in stent (n = 259). Po treh letih je bila stopnja restenoze z angiografijo v konvencionalni skupini TBCA 32%, v skupini s stentom pa 22%. Relativno zmanjšanje pogostosti restenoze je bilo 31% (p <0,01). V vstavitvijo žilne opornice skupini je bilo manjše potrebe po ponovne revaskularizacije miokarda (10 vs 20,6% v skupini normalne TBCA, p <0,01), ki je povezan z nižjo incidenco ponovitve angine v vstavitvijo žilne opornice pasu.
Po študijah stresu (n = 407) v vstavitvijo žilne opornice skupini (n ~ 205) restenorirovaniya frekvenca nižja kot pri konvencionalnem TBCA skupine (n = 202), - 31,6 proti 42,1% (p <0,01 ). Prednost z običajnim plastični kirurgiji ožilja opornico, preden v primeru restenoze na mestu TBCA REST je bila dokazana v študiji, v kateri so randomizirali 383 bolnikov z restenoze da vstavitvijo žilne opornice ali ponovno perkutano transluminalno koronarno angioplastiko. Angiografsko ugotovljena ponavljajoča se restenoza je bila v skupini s stentiranjem nižja za 18% (18 vs 5.32%, p <0,03). Ponavljajoče miokardno revaskularizacijo, ki je pokazatelj klinično pomembne restenoza zahteva tudi bistveno manj v skupini bolnikih z vstavitvijo žilne opornice (10 vs 27%, p <0,001). Tako so bili najboljši rezultati z uporabo stentiranja dokazani ne samo na avtohtonih arterijah, ampak tudi v primeru intervencije za restenozo, ki se je razvila po TBA.
Restenoza po implantaciji odkritega stenta (NPC)
Čeprav so nepremazani koronarnih stentov zmanjšano pojavnost restenoza primerjavi TBCA 30-40%, 17 -32% bolnikov, tudi po vstavitvijo žilne opornice restenoze že razvit v notranjosti tulca, ki zahteva revaskularizacije. Mehanizem razvoja intrinzične stenoze (HRV) se razlikuje od tistega v TBA. Po vstavitvijo žilne opornice restenoza glavni prispevek k temu, da nastanek neointime, namesto negativno preoblikovanje kot v TBCA, ki je na mesto implantacije stenta praktično odsotni. Neointima nastane zaradi migracije in proliferacije gladkih mišičnih celic, ki proizvajajo zunajcelični matriks, ki skupaj s celicami tvori neointima. Poleg tega je pri bolnikih z diabetesom pomembna tudi obstojnost tromba v mestu stentiranja.
Glavni Razvrstitev-stent stenoza (HRV) je razvrstitev spremembe MEHRAN, ki vključuje štiri vrste glede na obseg in resnostjo lezij: I HRV tip - lokalno (<10 mm dolžine), tipa II - razpršeno (> 10 mm v dolžino), tip III - proliferativna (> 10 mm in se razteza čez stent) in IV tipa HRV, ki vodi do okluzije. Prvi tip je razdeljen na podtipe glede na lokacijo v stenta: 1a - iz zavoja ali med stenta, 1b - rob, 1c - znotraj opornice, 1d - multifokalne.
Dejavniki tveganja za razvoj orožja za množično uničevanje so intervencijski pas veno cepljenk, kronični zapora, delto lezije, premer manjša plovila, prisotnost ostankov stenoze, opornice glede orožja za množično uničevanje, majhen premer postprotsedurny plovilo, PNA poraz, velika dolžina stent, prisotnost sladkorne bolezni, implantacije za več opornic v enem porazu . Obstajajo navedbe o vplivu genetskih faktorjev, zlasti glikoprotein IIIa polimorfizem in genske mutacije methylenetetrahydrofolate reduktazni - gena za interlevkin-1. Pri roba stent restenoza je pomemben dejavnik tveganja za aterosklerotične lezije, izražena v stentiruemom segmentu.
Pretežno se pojavijo restenoza v prvih 6-8 mesecih. Po perkutani koronarni intervenciji. Pri večini bolnikov ob istem času obstajajo klinični simptomi. Ponavadi se HRV manifestira kot ponovitev angine pektoris. Manj pogoste (11-41% primerov) je nestabilna angina. Pri 1-6% bolnikov se razvije AMI. Tako je najpogostejši vzrok angine v 1-6 mesecih. Po stentiranju je razvoj HRV, ki praviloma zahteva ponovljeno revaskularizacijo. Obstaja več načinov zdravljenja HRV. Konvencionalno TBA lahko izvedemo, kar vodi do nadaljnjega odpiranja stenta (56-odstotni prispevek k končnemu povečanju premera posode) in tudi potisne neointim skozi stentne celice (44-odstotni prispevek k povečanju končnega premera). Vendar pa se v večini primerov na mestu posega opazuje preostala restenoza (v povprečju 18%). Poleg tega je potrebno po TBCA revaskularizacije pri 11% primerov, pogosto pri bolnikih z multivessel boleznijo, nizko frakcije levega prekata, pri posegih na venskih spojev prvi ali zgodnje pogostnost pojavov HRV. Tveganje razvoja ponovnega HRV po TBCA je odvisno tudi od vrste lezije in se giblje od 10% pri lokalni restenozi na 80% z invazivno okluzijo. Implantacija NPC namesto HRV ne zmanjša tveganja ponovitve v primerjavi s samo TBA.
Druga metoda je zdravljenje HRV brahiterapijo, ki obsega dajanje radioaktivnega vira lumnu koronarnih arterij, ki preprečuje proliferacijo gladkih mišičnih celicah in temu ustrezno zmanjša tveganje restenoza. Kljub temu so visoki stroški opreme, tehnična kompleksnost postopka in povečana pogostnost pozne stentne tromboze (TC) skoraj popolnoma izključili brahiterapijo iz klinične uporabe.
Revolucionarni trenutek zdravljenja VRS je bil uvedba stentov, ki povzročajo drog. V primerjavi z nativno NNR v primeru, da zmanjšajo arterijski 70-80% nevarnost VSF prvih podatkov o učinkovitosti SLP pri bolnikih z že razvite HRV smo ga dobili pri bolnikih registracijo TAXUS III, pri čemer uporablja SPG1 pri teh bolnikih po 6 mesecih. Je bila stopnja recidiva HRV le 16%, kar je nižje kot v prej omenjenih študijah s TBA. V registru TRUE, ki je vključeval bolnike po implantaciji ATP za restenozo NPC, je bil po 9 mesecih. Ponavljajoča revaskularizacija je zahtevala manj kot 5% bolnikov, večinoma s sladkorno boleznijo in ACS. TROPSKI V študiji so primerjali pojavnost restenoze pri bolnikih po implantaciji na mestu restenoze DES Data Research GAMMA I in gama II, v kateri je E, kot je metoda zdravljenja uporablja Brahiterapevtskimi. Po 6 mesecih. Incidenca restenoze je bila v skupini ATP bistveno nižja (9,7 vs 40,3%, p <0,0001). Pomembno je, da je bila pogostnost tromboze žilne opornice miokardni infarkt tudi nižja v skupini ATP (TS 0,6% proti 3,9; p = 0,08; MI - 1,8 proti 9,4%, p = 0.004). Prednost ATP predhodnega brahiterapijo je bil potrjen v randomizirani SISR študiji, v kateri so bili 384 bolniki s sedežem HRV v HPC randomizirani ATP ali Brahiterapevtskimi implantacije. Po 9 mesecih. Potreba po ponovne revaskularizacije bila večja po brahiterapijo (19,2%) kot v skupini vsadi PCA (8.5%), kar kaže pogosteje ponovitev restenoze. Po treh letih se je ohranila prednost ATP v smislu zmanjšanja potrebe po ponavljajoči revaskularizaciji za ponovitev stent restenoze (19 proti 28,4%). Med incidenco tromboze med skupinami ni bilo bistvene razlike.
Glavni dejavniki za ponovitev HRV pri bolnikih z NPC v primeru implantacije ATP so majhnega premera posoda (<2,5 mm), difuzni tip restenoze, kot tudi prisotnost kronično ledvično odpovedjo, ki potrebujejo dializo. V randomiziranem preskušanju TAXUS V ISR je SPP dokazal tudi visoko učinkovitost pri zdravljenju HRV, s čimer se je hitrost recenzacije restenoze zmanjšala za 54% v primerjavi z brahiterapijo.
Randomizirane študije so bile opravljene tudi v primerjavi z učinkovitostjo TBA za implantacijo HRV in SLP. V randomizirani študiji o RIBS-II po 9 mesecih. Ponavljajoča se restenoza je bila 72% manj pogosta po implantaciji SLP kot po TBA, kar je zmanjšalo potrebo po ponovljeni revaskularizaciji s 30 na 11%. V študiji ISAR DESIRE je bila učinkovitost TBA v HRV primerjana z implantacijo SPP ali ATP. Po 6 mesecih. Izkazalo da sta BLT preprečitev restenoze učinkoviteje kot TBCA (stopnja razvoja je bila 44,6% na TBCA, 14,3% v skupini ATP in 21,7% v skupini CPR), ki je zmanjšal potrebo po ponovne revaskularizacije. Pri neposredni primerjavi s PPS in ATP se je izkazalo, da ATP zmanjšajo potrebo po ponovnem revaskularizaciji bistveno bolj učinkovito kot PPS (8 proti 19%). Tako implantacija SLP zmanjša pogostnost periodičnega HRV NPS v primerjavi z obema TBCA in brahiterapijo, ki zmanjša število ponoviti počne PCI, torej postopek implantacije izbire pri teh bolnikih.
Restenoza po implantaciji stenta, ki eluira zdravilo (SLP)
Kljub 70- do 80-odstotnemu zmanjšanju pojavnosti intra-stenalne stenoze pri uporabi SLP v primerjavi z NPC-ji, niso mogli popolnoma izključiti razvoja tega jaatrogenega učinka stentiranja. Njegova splošna frekvenca ostaja v povprečju manj kot 10%. Poleg kvantitativnega zmanjšanja pojavnosti restenoze so znatno spremenili vrsto restenoze, ki se pojavlja. Torej, po implantaciji SLP je restenoza praviloma osrednja. Klinično, kot v primeru NPS, se najpogosteje kaže kot relaps stabilne angine pektoris (77%), manj pogosto (8%), je asimptomatičen. V 5% primerov kaže nestabilno angino pektoris, pri 10% - prvi simptom je ne-Q-miokardni infarkt. Glavni dejavniki razvoja SLP restenoze so sladkorna bolezen tipa 2, majhen premer plovila, pa tudi obseg lezije. Jasna priporočila glede upravljanja takšnih bolnikov ne. Alternativa je ponovna implantacija SLP (istega tipa ali drugega tipa), izvajanje TBA ali brahiterapije. Povprečna pogostost razvoja restenoze med implantacijo druge SLP je 24%, medtem ko je enaka pri implantaciji iste vrste SLP ali druge.


 [
[