Medicinski strokovnjak članka
Nove publikacije
Genetski in presnovni vidiki patogeneze osteoartritisa
Last reviewed: 08.07.2025

Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.
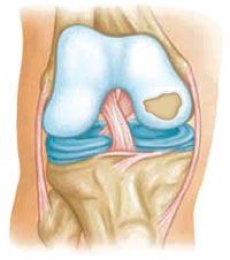
Vloga mehanskih dejavnikov pri patogenezi osteoartritisa je neizpodbitna, vendar obstajajo prepričljivi dokazi, da se nekatere oblike osteoartritisa dedujejo po Mendelovih zakonih. Dedne osteoartropatije lahko razdelimo na:
- primarni generalizirani osteoartritis (PGAO),
- artropatije, povezane s kristali,
- prezgodnja osteoartritis zaradi dedne osteohondrodisplazije.
Leta 1803 je W. Heberden opisal "rahlo goste bezgavke, velikosti majhnega graha" na hrbtni površini distalnih interfalangealnih sklepov rok. Ta simptom po mnenju avtorja loči osteoartritis od drugih bolezni sklepov, vključno s protinom. J. Hayagarth (1805) je razširil klinični opis Heberdenovih bezgavk in opozoril na njihovo pogosto povezavo z artrozo drugih lokalizacij. Kasneje je Bouchard opisal podobne bezgavke na hrbtni površini proksimalnih interfalangealnih sklepov rok. W. Osier je z izrazom "Heberdenove in Bouchardove bezgavke" razlikoval med "hipertrofičnim artritisom" in "deformirajočim artritisom" (1909). Leta 1953 sta R. M. Stecher in H. Hersh odkrila razširjenost Heberdenovih bezgavk med družinskimi člani in ugotovila, da se dedujejo avtosomno dominantno. Nadaljnje študije po odkritju R. M. Stecherja in H. Hersha so razkrile povezavo Heberdenovih in Bouchardovih bezgavk z degenerativnimi lezijami drugih sklepov. Na podlagi podatkov kliničnega pregleda in HLA-tipizacije so JS Lawrence (1977) in JS Lawrence ter sodelavci (1983) predlagali prisotnost poligenskega dedovanja in ne le okvare enega samega gena.
Fenotipski spekter dedne osteoartroze se zelo razlikuje od blagih oblik, ki postanejo klinično očitne šele v pozni odrasli dobi, do zelo hudih oblik, ki se pojavijo v otroštvu. Tradicionalno so bile vse te oblike razvrščene kot sekundarna osteoartritis. Zdaj je znano, da nekatere od teh fenotipov povzročajo mutacije v genih, ki kodirajo makromolekule zunajcelične mase sklepnega hrustanca (ECM), ki motijo celovitost hrustančne matrice ter regulacijo proliferacije hondrocitov in izražanja genov. Te dedne bolezni predstavljajo ločeno podskupino osteoartritisa, ki se razlikuje od sekundarne osteoartroze.
Razlike med dedno in sekundarno osteoartritisom (po Williamsu CJ in Jimenezu SA, 1999)
Dedna osteoartritis |
Sekundarna osteoartritis |
|
Etiologija |
Mutacija genov, izraženih v sklepnem hrustancu |
Različne dedne in pridobljene bolezni |
Patogeneza |
Poškodba strukturnih ali funkcionalnih komponent sklepnega hrustanca |
Sekundarne manifestacije bolezni, ki ne prizadenejo vedno le sklepnega hrustanca |
Zdravljenje |
Genska terapija je morda mogoča za odpravo genske napake |
Zdravljenje osnovne bolezni |
Hondrodisplazija/osteohondrodisplazija je skupina klinično heterogenih bolezni, za katere so značilne nepravilnosti v rasti in razvoju sklepnega hrustanca in rastne plošče. Nekatere Crohn-ove bolezni/OKM vodijo do zgodnjega razvoja osteoartritisa, za katerega je klinično značilen hud potek. Med njimi lahko ločimo naslednje bolezni:
- spondiloepifizna displazija (SED),
- Stiklerjev sindrom,
- displazija Knista,
- multipla epifizna displazija (MED),
- metafizna hondrodisplazija (MCD),
- nekatere oto-spondilo-meta-epifizne displazije (OSMED).
Dedne displazije, za katere je značilen zgodnji pojav osteoartritisa (po Williamsu CJ in Jimenezu SA, 1999)
Bolezen |
Lokus |
Vrsta dedovanja |
Mutiran gen |
Vrsta mutacije |
Zgodnji osteoartritis s poznim nastopom SED (OAR)* |
12q13.1–q13.2 |
PEKEL |
STOL 2 A, |
Zamenjava, vstavljanje, brisanje baz |
Sticklerjev sindrom (STL1) |
12q13.1–q13.2 |
PEKEL |
COL2A1 |
Zamenjava podnožja, vstavljanje |
Sticklerjev sindrom (STL2) |
6p21.3 |
PEKEL |
KOLA |
Vstavljanje, brisanje |
Sticklerjev sindrom |
1p21 |
PEKEL |
KOLA |
Zamenjava podnožja |
Wagnerjev sindrom |
12q13.1–q13.2 |
PEKEL |
COUA, |
Zamenjava podnožja |
OSMED |
6p21.3 |
Razširjena resničnost |
KOLA |
Zamenjava podnožja |
Marshallov sindrom |
1p21 |
PEKEL |
KOLA |
Vstavi |
Knista displazija |
12q13.1–q13.2 |
PEKEL |
KOLA |
Vstavljanje, brisanje |
M3fl(EDM1) |
19p13.1 |
PEKEL |
KOMP |
Zamenjava podnožja |
SREDNJE (EDM 2) |
1р32,2-рЗЗ |
PEKEL |
KOLA |
Vstavi |
MCDS |
6q21–q22.3 |
PEKEL |
KOLA |
Zamenjava, delecija baz |
MCDJ Jansen |
Зр21.2–р21.3 |
PEKEL |
PTHR, |
Zamenjava podnožja |
*Simboli lokusov so navedeni v oklepajih; AD - avtosomno dominantno; AR - avtosomno recesivno.
Spondiloepifizna displazija
Spondiloepifizne displazije (SED) vključujejo heterogeno skupino bolezni z avtosomno dominantnim tipom dedovanja, za katere je značilen nenormalen razvoj aksialnega okostja in hude spremembe epifiz dolgih cevastih kosti, kar pogosto povzroča pritlikavost. SED ima pogosto hud klinični potek, ki ga spremlja skrajšanje telesa in v manjši meri okončin.
Pri oblikah EDS, ki se pojavijo v poznejši starosti, je fenotip pogosto malo spremenjen in se klinično ne pojavi vse do adolescence, ko se razvije huda osteoartroza. Deformacija ledvene hrbtenice se lahko kaže kot zoženje medvretenčnih ploščic, platispondilija in blaga kifoskolioza. Zaznajo se tudi anomalije epifiz v perifernih sklepih in zgodnje degenerativne spremembe v njih. Najbolj stalen znak okvare perifernih sklepov je sploščenost sklepnih površin gleženjskega in kolenskega sklepa ter sploščenost interkondilarnega žleba stegnenice. Anomalije glave in vratu stegnenice se pogosto odkrijejo z razvojem osteoartroze kolčnega sklepa, ki se kaže v adolescenci.
Ker je kolagen tipa II glavna sestavina zunajcelične mase hialinskega hrustanca (ECM), se domneva, da je gen, ki ga kodira, COL1A, vzrok za EDS. Prvi opis genetske povezave med fenotipom zgodnje osteoartroze, povezane s poznim nastopom EDS, in genom prokolagena tipa II, COL 2 A, sega v leto 1989 in 1990. Prvo poročilo o mutaciji COL 2 A pri sorodnikih z zgodnjim osteoartritisom, povezanim s poznim nastopom EDS, je vključevalo zamenjavo baze Arg519>Cys. Do danes so bile identificirane še štiri družine s podobnimi mutacijami. Pri članih druge družine z zgodnjim OA in blagim EDS so ugotovili zamenjavo baze Arg75>Cys, čeprav fenotip EDS pri članih te družine ni podoben fenotipu družine z zamenjavo arginina s cisteinom na položaju 519. Druge mutacije COL 2 A-Gly976>Ser, Gly493>Ser so bile najdene tudi pri članih družin z EDS. J. Spranger in sodelavci (1994) so uporabili izraz "kolagenopatija tipa 11" za opis dednih bolezni hrustančnega tkiva s primarno mutacijo v genu prokolagena tipa II COL1A.
Klasična oblika Sticklerjevega sindroma
Prvič ga je leta 1965 opisal GB Stickler s sodelavci, ki so ga poimenovali dedna artro-oftalmopatija. Sindrom, ki ga je opisal GB Stickler, je bil značilen za okvaro vida in hudo degenerativno bolezen sklepov, ki se običajno razvije v tretjem ali četrtem desetletju življenja. Gre za avtosomno dominantno motnjo z incidenco približno 1 na 10.000 živorojenih otrok. Klinična slika vključuje kratkovidnost, progresivno gluhost, razcepljeno nebo, hipoplazijo spodnje čeljusti (Pierre-Robinova anomalija) in hipoplazijo epifiz. V neonatalnem obdobju rentgenski posnetki bolnikov s Sticklerjevim sindromom razkrijejo povečane epifize, predvsem proksimalni femur in distalni del golenice. Med rastjo se razvije epifizna displazija, ki se kaže z nepravilno osifikacijo epifiz in posledičnimi degenerativnimi spremembami.
Ker se COL 2 A izraža v sklepnem hrustancu in steklovini zrkla, je bil pojav Sticklerjevega sindroma povezan s patologijo tega gena. Vendar pa je pregled več družin s Sticklerjevim sindromom pokazal, da nimajo vse družine bolezni, povezane s COL 2 A. Ta oblika bolezni se imenuje Sticklerjev sindrom tipa I (simbol lokusa STL1).
Spekter kliničnih manifestacij Sticklerjevega sindroma se zelo razlikuje in do danes je bilo identificiranih več fenotipov. Med njimi je Wagnerjev sindrom, za katerega je značilna prevladujoča poškodba zrkla; osteoartritis pri Wagnerjevem sindromu se praktično nikoli ne razvije, čeprav je bila pri bolnikih ugotovljena mutacija gena COL 2 A (bazna substitucija Gly67>Asp). Ni jasno, zakaj takšna mutacija COL ogroža le delovanje steklovine in ne vpliva na hialinski hrustanec.
Druga oblika Sticklerjevega sindroma je tako imenovana nizozemska varianta; zanjo so značilne vse klasične manifestacije sindroma, razen okvare vida. HG Brunner in sodelavci (1994) so pokazali, da je nizozemski fenotip Sticklerjevega sindroma povezan z mutacijo v genu COL,,A2 : dominantna mutacija je delecija 54 baznih parov, ki ji sledi delecija eksona. M. Sirko-Osadsa in sodelavci (1998) so poročali o drugi družini, ki ni povezana s tisto, ki so jo opisali prejšnji avtorji, s podobnim fenotipom in mutacijo v genu COL,,A2 ( delecija 27 baznih parov), kar potrjuje podatke HG Brunnerja in sodelavcev (1994). Ta varianta se imenuje Sticklerjev sindrom tipa II (simbol lokusa STL1).
Nedavno je bil pri članih družine s patologijo steklovine in mrežnice identificiran tretji lokus Sticklerjevega sindroma, ki se fenotipsko bistveno razlikuje od sprememb, opaženih pri "klasični" varianti sindroma. Pri članih te družine je bila odkrita mutacija v genu COL2A| (bazna substitucija Gly97>Val). Seveda so za potrditev ugotovitev A. J. Richardsa in sodelavcev potrebni novi opisi primerov tega feno- in genotipa Sticklerjevega sindroma.
Nozološka povezava med Marshallovim sindromom in klasično različico Sticklerjevega sindroma je predmet razprav že dolgo. Danes je Marshallov sindrom razvrščen kot ločen fenotip predvsem zaradi izrazitejše deformacije obraznega skeleta, čeprav je poškodba perifernih sklepov podobna kot pri Sticklerjevem sindromu tipa I. Pri Marshallovem sindromu se osteoartritis kolenskih sklepov in ledvenokrižne hrbtenice začne po 30 letih. Vzrok sindroma je mutacija v genu za kolagen tipa IX COL n A1.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ]
OSMED
Ta fenotip je bil opisan v nizozemski družini, v kateri so se v adolescenci pojavile degenerativne spremembe v sklepih, podobne osteoartrozi, in so prizadele predvsem kolčne, kolenske, komolčne in ramenske sklepe; ugotovljene so bile tudi nenavadne obrazne poteze, povečana ledvena lordoza, povečani interfalangealni sklepi in izguba sluha, vendar niso bile odkrite nobene vidne anomalije (Vikkula M. et al., 1995). Raziskovalci so odkrili mutacijo v genu, ki kodira α2 -verigo kolagena tipa II COL,, A2.
Knista displazija
Zanj so značilni skrajšanje trupa in okončin, sploščenost obraza in nosnega korena, eksoftalmus in hude nepravilnosti sklepov. Pri bolnikih s Kniestovim sindromom se sklepi, ki so običajno veliki od rojstva, v otroštvu in zgodnji adolescenci še naprej povečujejo. Pogosto imajo tudi kratkovidnost, izgubo sluha, razcepljeno nebo in klobučnjačo; večina bolnikov zgodaj razvije hude degenerativne spremembe, še posebej izrazite v kolenskih in kolčnih sklepih. Rentgenske slike hrbtenice razkrivajo sploščenost in znatno podolgitev vretenc in platispondilozo. Dolge cevaste kosti so deformirane kot utež, osifikacija epifiz pa je počasna. V sklepih rok so epifize sploščene, sklepne špranje pa zožene. Sklepni hrustanec je mehak, njegova elastičnost je zmanjšana; histološko v njem najdemo velike ciste (simptom "švicarskega sira"). Kniestov sindrom povzroča mutacija v genu za prokolagena tipa II COb2A1.
 [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ]
[ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ]
Multipla epifizna displazija (MED)
Heterogena skupina bolezni, za katere je značilen nenormalen razvoj rastnih plošč dolgih cevastih kosti, pa tudi zgodnja (ki se kaže v otroštvu) huda osteoartroza, ki prizadene tako aksialne kot periferne sklepe (najpogosteje kolenske, kolčne, ramenske in sklepe rok). Klinično se MED kaže kot bolečina in okorelost v sklepih, spremembe v hoji. Bolniki z MED imajo tudi minimalne spremembe v hrbtenici (različne stopnje sploščenosti vretenc), včasih je hrbtenica nedotaknjena. Značilna je tudi nizka rast bolnikov, čeprav se pritlikavost redko razvije. Vidni organ ni prizadet. MED vključuje več različic, na primer fenotip Fairbanks in Ribbing.
MED se dedujejo avtosomno dominantno z različnimi stopnjami penetracije. Ker je značilnost MED anomalija epifizne rastne plošče, se domneva, da te displazije povzroča okvara v genih, ki kodirajo makromolekule hrustanca rastne plošče. Izkazalo se je, da so s fenotipom MED povezani vsaj trije lokusi. Študije E. J. Weaverja in sodelavcev (1993), J. T. Hechta in sodelavcev (1992) so s seznama "krivcev" za MED izključile gene kolagena tipov II in VI, osrednji protein proteoglikanov in vezivni protein hrustanca. J. T. Hecht in sodelavci (1993) ter R. Oehelmann in sodelavci (1994) so odkrili povezavo med MED, pa tudi klinično povezanim sindromom psevdoahondroplazije, in pericentromerno regijo kromosoma 19. Nadaljnje študije so pri treh bolnikih z MED (simbol lokusa EDM1) odkrile mutacijo v genu, ki kodira protein hrustančnega oligomernega matriksa (OMMP). Ker so se vse tri mutacije pojavile v genski regiji, ki kodira domeno OMMP, ki veže kalcij, je verjetno, da je funkcija vezave kalcija te beljakovine bistvena za normalen razvoj hrustanca rastne plošče.
MD Briggs in sodelavci (1994) so poročali o nizozemski družini s fenotipom MED, povezanim z regijo kromosoma 1, ki vsebuje enega od genov kolagena tipa IX, COL1A1 (simbol lokusa EDM 2). Omeniti velja, da je bila najdena mutacija prvi dokaz o vlogi kolagena tipa IX, lokaliziranega na površini fibril kolagena II, pri ohranjanju celovitosti hialinskega hrustanca. M. Deere in sodelavci (1995) so pokazali, da fenotip Fairbanks ni bil genetsko povezan niti z lokusom EDM niti z lokusom EDM2, kar potrjuje heterogenost MED.
Metafizna hondrodisplazija (MCD)
Heterogena (opisanih je več kot 150 vrst) skupina dednih bolezni hialinskega hrustanca, ki se klinično kažejo kot zgodnja osteoartroza. Za MHD so značilne spremembe v kostnih metafizah. Klinično se kažejo kot nizka rast, skrajšani okončine, ukrivljene goleni in "račja" hoja. Bolniki z MHD kažejo tudi znake okvare drugih sistemov (na primer imunskega in prebavnega sistema). Opažena je neorganiziranost hrustanca rastne plošče, ki se histološko kaže kot skupki proliferiranih in hipertrofiranih hondrocitov, obdanih z odebeljenimi septami in neorganizirano matrico, ter kot prodiranje nekalcificiranega hrustanca v subhondralno kost.
Jansenov, Schmidov in McKusickov sindrom so najbolj raziskane bolezni mišično-skeletnega sistema (MHD). Podobni so si po značilnostih skeletnih anomalij, razlikujejo pa se po resnosti (Jansenov sindrom-McKusickov sindrom-Schmidov sindrom). Najpogostejši je Schmidov sindrom (simbol lokusa MCDS), ki se deduje avtosomno dominantno. Radiološko se sindrom kaže s coxa vara, skrajšanjem in ukrivljenostjo cevastih kosti, skodelicasto deformacijo metafiz (bolj izrazita v proksimalnem kot v distalnem delu stegnenice). Najbolj izrazite spremembe opazimo v rastnih ploščah dolgih cevastih kosti.
Pri bolnikih s Schmidovim sindromom je bilo opisanih vsaj 17 različnih vrst mutacij gena kolagena X. Kolagen X se izraža v hipertrofiranih hondrocitih rastnih plošč in je lahko vključen v procese osifikacije. Zato je mutacija v genu kolagena X COb2A1 najverjetnejši vzrok Schmidovega sindroma.
Otroci z Jansenovim sindromom imajo hiperkalcemijo, povišane ravni fosfata v urinu ter znižane ravni paratiroidnega hormona (PTH) in peptidov, povezanih s PT. Anomalija slednjega je verjetno odgovorna za razvoj Jansenovega sindroma. Leta 1994 so AS Karaplis in soavtorji objavili rezultate izvirne študije. Po motnji gena, ki kodira peptid, povezan s PT, v mišjih embrionalnih matičnih celicah so miši s pomanjkanjem tega alela takoj po rojstvu poginile. Ugotovili so, da imajo anomalijo v razvoju subhondralne kosti, oslabljeno rast hrustanca in zmanjšano proliferacijo hondrocitov. Leta 1995 so E. Schipani in soavtorji poročali o heterozigotni mutaciji v genu za receptor PTH pri bolniku z Jansenovim sindromom. Mutacija je bila sestavljena iz zamenjave baze Gys223>Arg, kar je povzročilo kopičenje cAMP; To pomeni, da ima aminokislina histidin na položaju 223 ključno vlogo pri prenosu signala. Kasneje so E. Schipani in sod. (1996) so poročali o treh drugih bolnikih z Jansenovim sindromom, od katerih sta imela dva podobno mutacijo, tretji pa je imel substitucijo TrА10>РrО.
Primarni generalizirani osteoartritis
Najpogostejša dedna oblika osteoartritisa je primarni generalizirani osteoartritis (PGOA), ki sta ga kot ločeno nozologijo prvič opisala JH Kellgren in R. Moore leta 1952. Klinično je za primarni generalizirani osteoartritis značilen pojav Bouchardovih in Heberdenovih bezgavk ter poliartikularnih lezij. Za primarni generalizirani osteoartritis je značilen zgodnji začetek manifestacije osteoartritisa in njegovo hitro napredovanje. Radiološko se primarni generalizirani osteoartritis ne razlikuje od nedednega osteoartritisa. Kljub temu, da je vprašanje etiopatogeneze primarnega generaliziranega osteoartritisa še vedno predmet razprav, študije kažejo na pomembno vlogo dedne predispozicije pri nastanku in napredovanju primarnega generaliziranega osteoartritisa.
Tako so JH Kellgren in sodelavci (1963) odkrili Boucharay-Heberdenove bezgavke pri 36 % moških sorodnikov in 49 % ženskih sorodnikov, medtem ko sta bili v splošni populaciji ti številki 17 oziroma 26 %. Pri posameznikih s primarno generalizirano osteoartritisom se pogosteje odkrijeta haplotip HLA A1B8 in izoforma MZ α1-antitripsina. V klasični študiji dvojčkov so TD Spector in sodelavci (1996) opravili radiografijo kolenskih in roknih sklepov pri 130 enojajčnih in 120 dvojajčnih dvojčkih zaradi sprememb, značilnih za osteoartritis. Izkazalo se je, da je bila skladnost radiografskih znakov osteoartritisa vseh lokalizacij 2-krat večja pri enojajčnih dvojčkih v primerjavi z dvojajčnimi dvojčki, prispevek genetskih dejavnikov pa se je gibal od 40 do 70 %. Študija nodularnega osteoartritisa, ki sta jo izvedla GD Wright in sodelavci... (1997) so pokazali zgodnji pojav bolezni, visoko resnost in negativno korelacijo med starostjo pojava bolezni pri bolnikih in starostjo spočetja njihovih staršev.
Med artropatijami, povezanimi s kristali, je odlaganje kristalov sečne kisline in kristalov, ki vsebujejo kalcij, v sklepni votlini družinsko predispozicijo.
Dedne artropatije, povezane s kristali (po Williamsu CJ in Jimenezu SA, 1999)
Bolezen |
Lokus |
Vrsta dedovanja |
Mutiran gen |
Vrsta mutacije |
Protin (HPRT)* |
Xq27 |
X-vezana |
HPRT1 |
Zamenjava, delecija baz |
Protin (PRPS) |
Xq22–q24 |
X-vezana |
PRPS1 |
Zamenjava podnožja |
Primarna pirofosfatna artropatija (CCAL1) |
5r15.1–r15.2 |
PEKEL |
? |
? |
Zgodnja pirofosfatna artropatija, povezana z 0A (CCAL2) |
8q |
PEKEL |
? |
? |
*Simboli lokusov so navedeni v oklepajih; AD – avtosomno dominantno.
Leta 1958 je D. Zintann S. Sitaj predstavil klinične opise patologije, ki so jo poimenovali "hondrokalcinoza", pri 27 bolnikih. Večina bolnikov je pripadala petim družinam, kar kaže na dedno komponento v etiopatogenezi bolezni. Kasneje sta D. McCarty in JL Hollander (1961) poročala o dveh bolnikih, pri katerih so sumili na protin z odlaganjem nonuratnih kristalov v sklepni votlini. Rentgenski pregled je razkril nenormalno kalcifikacijo hialinskega hrustanca številnih sklepov.
Radiografsko je bolezen odlaganja kristalov kalcijevega pirofosfat dihidrata ali pirofosfatna artropatija podobna sporadični osteoartritisi, vendar pogosteje prizadene sklepe, ki niso značilni za pogoste oblike osteoartroze (npr. metakarpofalangealni, skaforadialni, patelofemoralni kolenski sklepi). Pri pirofosfatni artropatiji se pogosteje oblikujejo subhondralne kostne ciste. Čeprav se v večini primerov hondrokalcinoza pojavi pred manifestacijo sekundarne osteoartroze, se lahko pri nekaterih posameznikih bolezen začne kot idiopatska osteoartroza, ki jo spremljajo presnovne motnje (hemokromatoza, hiperparatiroidizem, hipomagneziemija itd.).
Najverjetneje strukturne spremembe v zunajceličnem materialu sklepnega hrustanca povzročijo odlaganje kristalov kalcijevega pirofosfat dihidrata. AO Bjelle (1972, 1981) je ugotovil zmanjšanje vsebnosti kolagena in fragmentacijo kolagenskih vlaken v srednjem območju matrice sklepnega hrustanca pri članih švedske družine s pirofosfatno artropatijo. Ker ta območja niso vsebovala kristalov, so avtorji predlagali, da lahko opisana anomalija matrice predisponira k njihovemu odlaganju in razvoju degenerativnih sprememb v sklepih. Na podlagi študije sporadičnih primerov pirofosfatne artropatije so K. Ishikawa in sod. (1989), I. Masuda in sod. (1991) zaključili, da hondrokalcinozo povzroča mutacija v genih, ki kodirajo beljakovine zunajceličnega materiala. CJWilliams in sod. (1993), AJ Reginato in sod. (1994) so pri članih velike družine s kliničnim fenotipom hude zgodnje osteoartroze z ankilozo, poznim razvojem spondiloepifizne displazije in hondrokalcinoze hialina in fibrohrustanca odkrili heterozigotno mutacijo COL 2 A (bazna substitucija Argl5>Cys). Vendar se je izkazalo, da je bila pri članih te družine hondrokalcinoza sekundarna glede na osteoartritis.
Prav tako je bilo predlagano, da anorganske komponente zunajcelične matrike (ECM) prispevajo k nastanku kristalov. Na primer, hipomagneziemija povzroča hondrokalcinozo z zaviranjem encima pirofosfataze, kar posledično zmanjša raztapljanje kristalov. V sinovialni tekočini bolnikov s pirofosfatno artropatijo so odkrili povišane ravni anorganskih fosfatov. To in druga opažanja kažejo, da imajo bolniki s pirofosfatno artropatijo lokalno motnjo presnove pirofosfata. Opisan je bil encim nukleozid trifosfat pirofosfohidrolaza, ki je lahko vpleten v nastajanje kristalov pirofosfata na območju njihovega odlaganja v zunajceličnem matriku. Povišane ravni tega encima so odkrili v sporadičnih primerih pirofosfatne artropatije, vendar te nepravilnosti niso opazili pri družinskih oblikah bolezni (Ryan LM et al., 1986). Vendar pa so pri gojenju fibroblastov in limfoblastov bolnikov z družinsko pirofosfatno artropatijo odkrili povečanje vsebnosti anorganskih fosfatov, kar potrjuje tudi domnevo o vlogi motenj v lokalni presnovi pirofosfata pri patogenezi bolezni.
V zadnjih letih so se izvajali poskusi identifikacije genov, ki so "krivi" za pojav družinskih primerov pirofosfatne artropatije. Tako je analiza genskega materiala, pridobljenega od članov velike družine s pirofosfatno artropatijo (Maine, ZDA), pri kateri se je hondrokalcinoza razvila sekundarno zaradi hude, hitro napredujoče, nedisplastične osteoartroze, izključila povezavo med boleznijo in lokusom COL 2. Vendar pa so avtorji te študije ugotovili povezavo med preučevanim fenotipom pirofosfatne artropatije in lokusom, ki se nahaja na dolgem kraku kromosoma 8 (simbol lokusa CCAL). AG Hughes in sod. (1995) so ugotovili povezavo med fenotipom primarne hondrokalcinoze v družini iz Združenega kraljestva in lokusom CCAL1, ki je lokaliziran na kratkem kraku kromosoma 5 v regiji 5p15. Po CJ Williamsu in sod. (1996) je bil lokus CCAL1 pri članih argentinske družine s pirofosfatno artropatijo lociran nekoliko bolj proksimalno kot v prejšnjem primeru, v regiji 5p15.1. Podoben genotip so našli pri članih družine iz Francije.
Podatki iz opisanih študij torej kažejo, da je družinska oblika pirofosfatne artropatije klinično in genetsko heterogena bolezen, ki jo lahko povzročijo mutacije v vsaj treh različnih genih.

